¿Qué es la Microbiota?
La microbiota se define como el conjunto de microorganismos (bacterias, virus, hongos, arqueas y protozoos) que habitan nuestro cuerpo. Estos billones de microbios viven en simbiosis, es decir, en beneficio mutuo con nuestras células. No importa solo un microorganismo en forma aislada, sino la red que conforman: un ecosistema metabólico y funcional complejo.
Los microorganismos colonizan diversos sitios anatómicos, como la piel, el tracto gastrointestinal, el tracto respiratorio, el tracto urogenital y la glándula mamaria.
El microbioma es el conjunto total de genes de los microorganismos que integran la microbiota; es decir, su paquete genético. Su análisis permite identificar qué microorganismos están presentes y conocer su potencial funcional.
El 95% de los microorganismos se ubican en el tracto gastrointestinal. En el intestino grueso se encuentra la mayor densidad microbiana y el ecosistema más complejo. En el estómago, en cambio, la microbiota es muy escasa debido a la acidez extrema y a las enzimas digestivas, que dificultan el crecimiento y la supervivencia de muchos microorganismos. En el intestino delgado comienza a aumentar progresivamente la cantidad y diversidad microbiana, alcanzando su máxima concentración en el intestino grueso.
La densidad microbiana varía a lo largo del tubo digestivo según el oxígeno, el pH y la capa de moco protector:
Oxígeno
Disminuye a lo largo del tracto gastrointestinal.
El colon se caracteriza por un ambiente predominantemente anaeróbico, condición que favorece el desarrollo de bacterias fermentadoras de sustratos no digeribles, como las fibras prebióticas.
pH intestinal
Aumenta gradualmente desde el estómago hacia el colon.
El pH ácido del estómago limita el crecimiento microbiano, mientras que el pH más elevado del colon favorece una mayor densidad y diversidad microbiana.
Capa de moco protector
Se incrementa hacia el intestino grueso.
Cumple un rol clave en la protección del epitelio intestinal y en el mantenimiento y refuerzo de las uniones estrechas, contribuyendo a la integridad de la barrera intestinal.
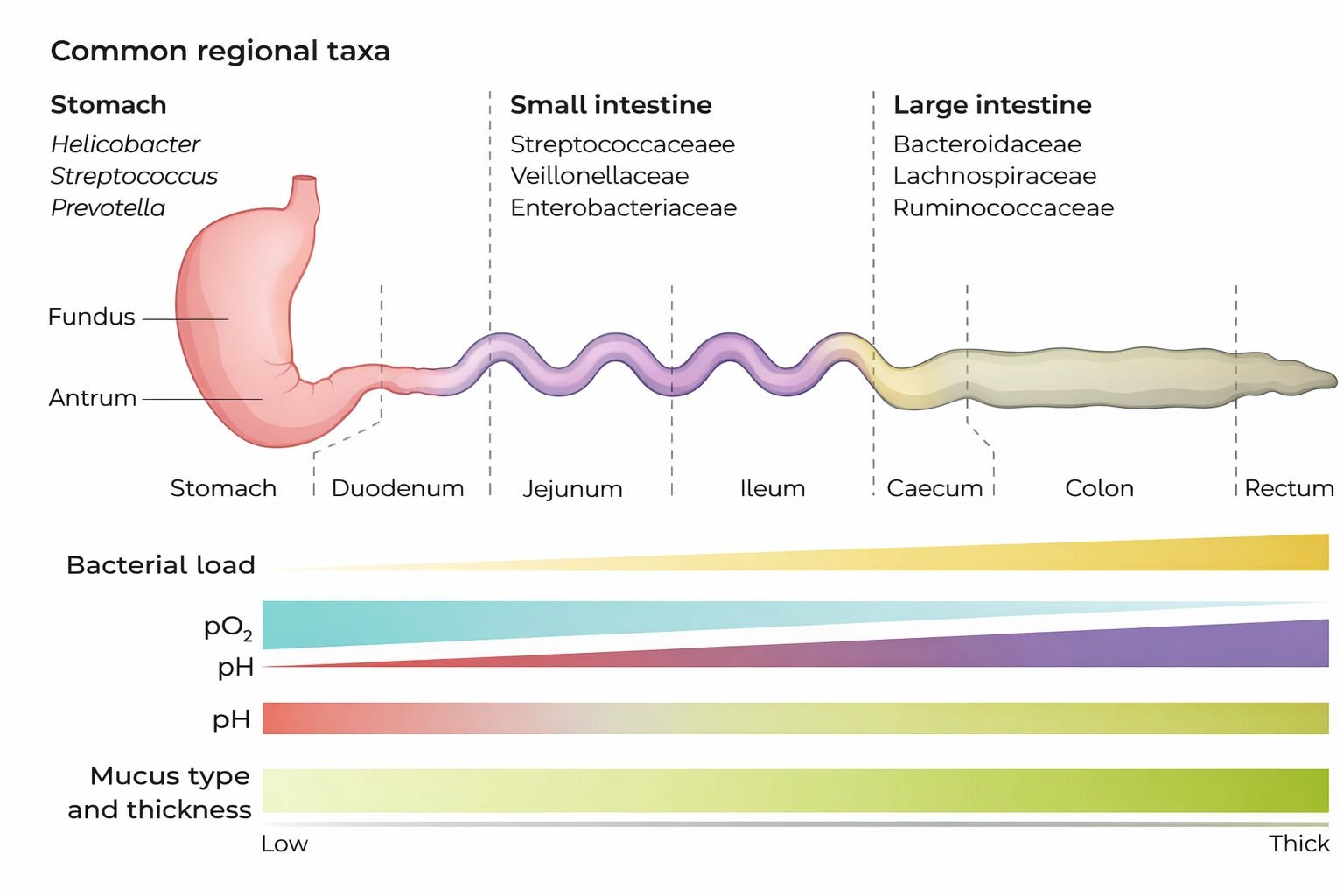
Hacer click sobre el cuadro para ampliar la imagen.
McCallum, G., & Tropini, C. (2024). The gut microbiota and its biogeography. Nature reviews. Microbiology.
Rol de la microbiota en la salud
La microbiota constituye un ecosistema metabólico y funcional complejo que cumple un papel central en el mantenimiento de la salud. Muchos de sus beneficios derivan de su actividad metabólica y de las sustancias que produce. Entre ellas se encuentran los ácidos grasos de cadena corta (AGCC) —acetato, propionato y butirato—, principales metabolitos generados por la fermentación colónica de fibras prebióticas como la inulina.
Funciones metabólicas y digestivas
Colabora en la degradación de compuestos que el intestino humano no puede procesar por sí solo. Se encarga de la fermentación de las fibras y carbohidratos no digeribles produciendo AGCC clave para la salud del colon y el metabolismo energético.
Eliminación de compuestos tóxicos
Muchas bacterias intestinales poseen enzimas capaces de metabolizar toxinas y algunas bacterias pueden unirse físicamente a metales pesados, micotoxinas, o toxinas bacterianas, evitando su absorción intestinal. Por ejemplo el Lactobacillus rhamnosus puede unirse a aflatoxinas, reduciendo su biodisponibilidad.
Protección frente a patógenos
Mediante mecanismos de exclusión limita su crecimiento compitiendo por nutrientes y nichos ecológicos. También produce bacteriocinas y ácidos orgánicos con efecto antimicrobiano.
Modulación inmunológica
Estimula el desarrollo del sistema inmune innato y adaptativo, influenciando tanto la maduración de células inmunitarias como la producción de citoquinas, también evita respuestas inflamatorias desmedidas.
Las células linfoides innatas (CLI) que se localizan en el epitelio intestinal están involucradas en el mantenimiento de respuestas inmunes apropiadas a los distintos microorganismos, potenciando la inmunidad adaptativa, y regulando la inflamación y la reparación de tejidos en la mucosa intestinal. Las funciones de las CLI también están reguladas por la microbiota.
Las interacciones entre la microbiota y las células del sistema inmune innato se producen a través de receptores de reconocimiento de patrones moleculares microbianos (TLR, NODs, inflamasomas, etc.) o de metabolitos (triptófano, indoles, butirato) producidos por la microbiota. Estos estímulos activan tanto las funciones de barrera anteriormente descritas, como la síntesis de otros mediadores (citoquinas, moléculas co-estimuladoras, etc.) que regulan la respuesta de células inmunes especializadas del tejido linfoide asociado al intestino, coordinando sus acciones para evitar la invasión de patógenos y favorecer el desarrollo de tolerancia a antígenos inocuos.
Mantenimiento de la barrera intestinal
La microbiota ejerce un efecto trófico sobre el epitelio intestinal, favoreciendo la proliferación de las células epiteliales y el mantenimiento de las uniones estrechas. La microbiota además es clave para que se produzca la capa de moco que protege el epitelio intestinal favoreciendo su integridad.
Síntesis de compuestos bioactivos y neuroactivos
La microbiota intestinal participa activamente en la síntesis de compuestos bioactivos esenciales, como vitaminas del complejo B y vitamina K, fundamentales para la coagulación y el metabolismo.
Además, interviene de forma directa o indirecta en la síntesis de compuestos neuroactivos, incluidos distintos neurotransmisores (serotonina, dopamina, ácido γ-aminobutírico [GABA], etc.) que influyen en las funciones cerebrales, el comportamiento, el metabolismo y la inmunidad.
La influencia de la microbiota en la síntesis de serotonina es particularmente relevante, ya que hasta un 90% de este neurotransmisor —que ejerce funciones clave a nivel central y periférico— se sintetiza en el intestino. A nivel del sistema nervioso central, la serotonina regula el estado de ánimo, el apetito y las funciones cognitivas; a nivel intestinal, regula la inflamación y la motilidad. La microbiota intestinal puede estar implicada tanto en la reducción de los niveles de serotonina, por su capacidad de metabolizar el triptófano que actúa como precursor, como en su producción, estimulando la expresión de los genes (triptófano 1 hidroxilasa) implicados en su síntesis. La modulación microbiana de la biosíntesis de serotonina y de la expresión de sus receptores mitiga la inflamación intestinal y los síntomas depresivos.
Asimismo, diversas bacterias intestinales codifican tirosinasas capaces de transformar la tirosina en L-dihidroxifenilalanina (L-DOPA), que a su vez conduce a la síntesis de catecolaminas como dopamina, norepinefrina y epinefrina. La dopamina cumple una función importante en el sistema de recompensa, implicado en la regulación del comportamiento alimentario y del estado de ánimo.
Por su parte, el GABA es producido por diversas bacterias intestinales a través de la descarboxilación del glutamato por acción de la enzima glutamato descarboxilasa, implicada en la tolerancia al pH ácido y el mantenimiento de la homeostasis intracelular bacteriana. El GABA es un importante neurotransmisor con efectos inhibidores en el cerebro, y su disfunción está implicada en enfermedades como el autismo y la esquizofrenia.
Ácidos grasos de cadena corta: metabolitos clave de la fermentación microbiana
Aunque durante años se consideró a los AGCC simplemente como una fuente energética para los colonocitos, hoy se los reconoce como mediadores clave en la comunicación entre la microbiota intestinal y el organismo, desempeñando un papel central en el mantenimiento de la homeostasis local y sistémica.
Rol de los AGCC sobre la barrera intestinal
La mucosa intestinal está recubierta por una capa de moco rica en mucinas que actúa como barrera física frente a bacterias y virus, ácidos biliares, enzimas digestivas y sustancias irritantes de la dieta. Esta capa mantiene a las bacterias separadas del epitelio, limita la adhesión de patógenos, reduce la translocación de endotoxinas bacterianas como el lipopolisacárido (LPS) y disminuye la activación inflamatoria innecesaria.
Regulan la secreción de moco
El butirato constituye el principal sustrato energético de los colonocitos y es el regulador más potente de la secreción de moco, contribuyendo al refuerzo de las uniones estrechas. Sin esta capa mucosa, el epitelio sería altamente vulnerable a lesiones y erosiones. La producción de inmunoglobulina A secretora (IgA) representa otro mecanismo defensivo clave, ya que limita el acceso de bacterias a la mucosa mediante su neutralización y favorece su eliminación. Asimismo, los macrófagos fagocitan y eliminan los microorganismos que eventualmente atraviesen el epitelio intestinal. En conjunto, esta red estructural e inmunológica mantiene la integridad funcional de la barrera intestinal.
Disminuyen el pH luminal
Además de mantener la integridad estructural de la barrera, los AGCC contribuyen a disminuir el pH luminal, creando un entorno menos favorable para microorganismos patógenos. También estimulan la motilidad intestinal y modulan activamente la respuesta inmune, reduciendo la producción de citoquinas proinflamatorias y promoviendo un perfil inmunológico antiinflamatorio.
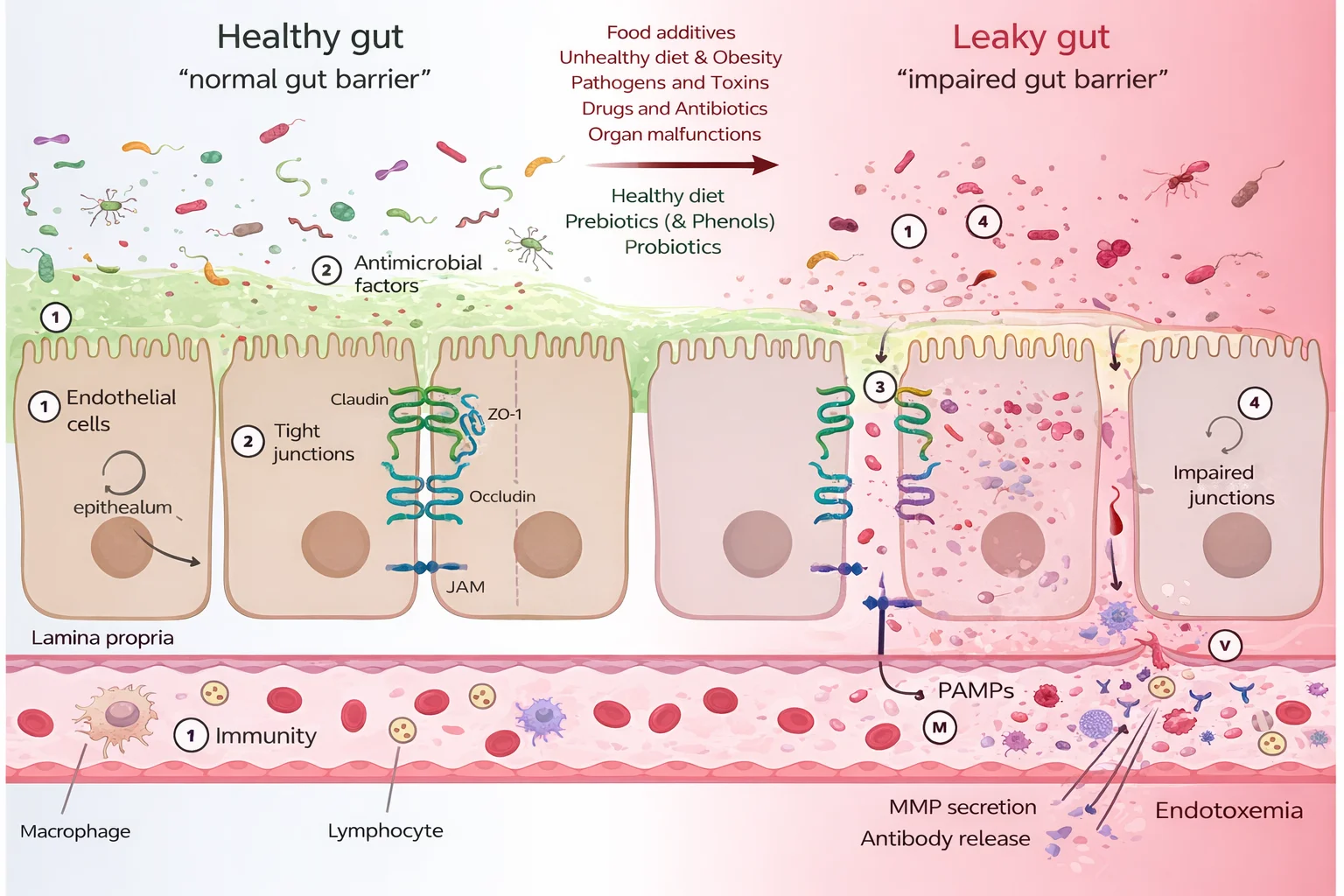
Hacer click sobre el cuadro para ampliar la imagen.
Journal of Endocrinology 248, 2; 10.1530/JOE-20-0473
Impacto sobre la Permeabilidad Intestinal
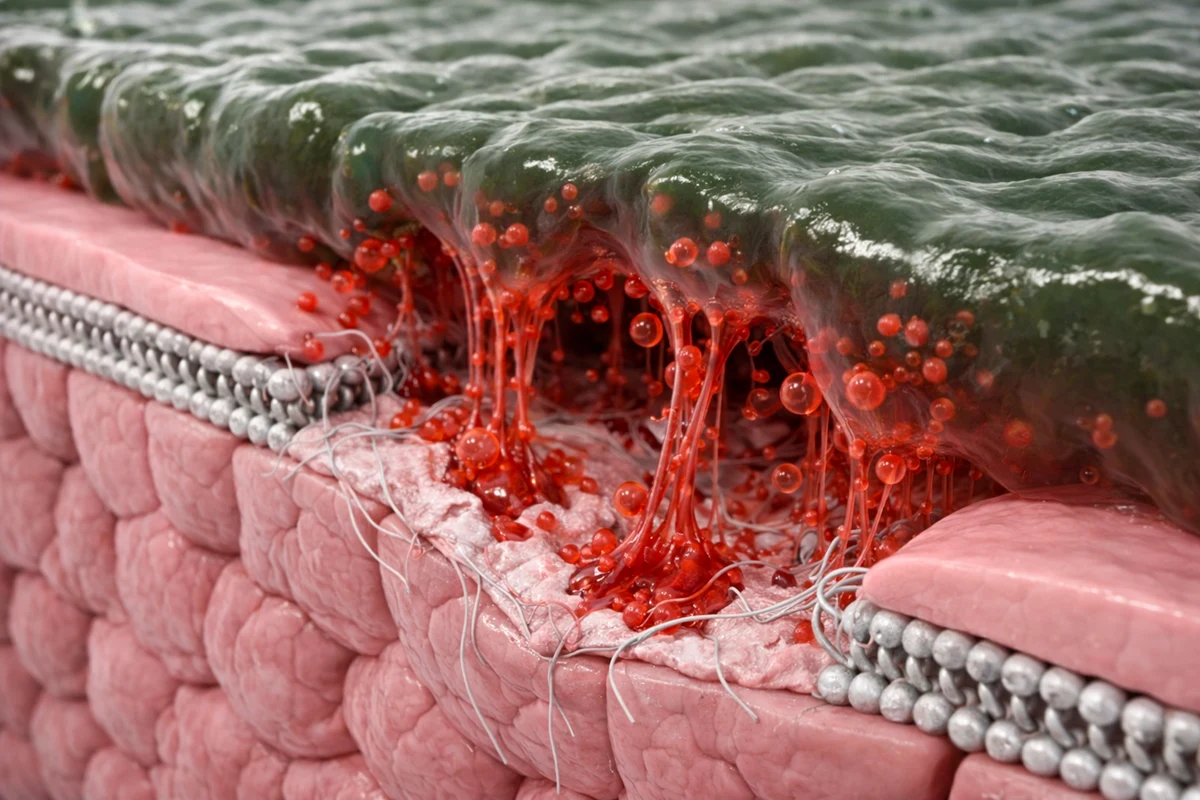
Cuando disminuyen las bacterias productoras de AGCC, esta red defensiva se debilita. La barrera epitelial pierde cohesión, se compromete la integridad y se desregula la respuesta inmune, aumentando la permeabilidad intestinal y facilitando el paso de bacterias y de sus componentes hacia la circulación sistémica.
Entre estos componentes, el LPS, molécula que forma parte de la membrana externa de las bacterias Gram negativas activa receptores de reconocimiento en células inmunes, promoviendo la producción de citoquinas proinflamatorias. Este proceso favorece endotoxemia metabólica y la instauración de un estado inflamatorio sistémico persistente de bajo grado.
Inflamación crónica
Este tipo de inflamación crónica de bajo grado no solo se asocia a alteraciones metabólicas, sino también al envejecimiento biológico. La inflamación crónica puede afectar procesos fisiológicos como la síntesis de proteínas musculares, contribuyendo a la sarcopenia y a la fragilidad, y constituye un eje fisiopatológico común en múltiples enfermedades crónicas.
Manifestaciones clínicas sistémicas
En conjunto, la alteración de los AGCC configura un mecanismo central que vincula la disbiosis intestinal con el desarrollo y progresión de enfermedades metabólicas, inmunológicas y degenerativas de alta prevalencia. Desde este punto de partida intestinal se comprenden múltiples manifestaciones clínicas sistémicas.
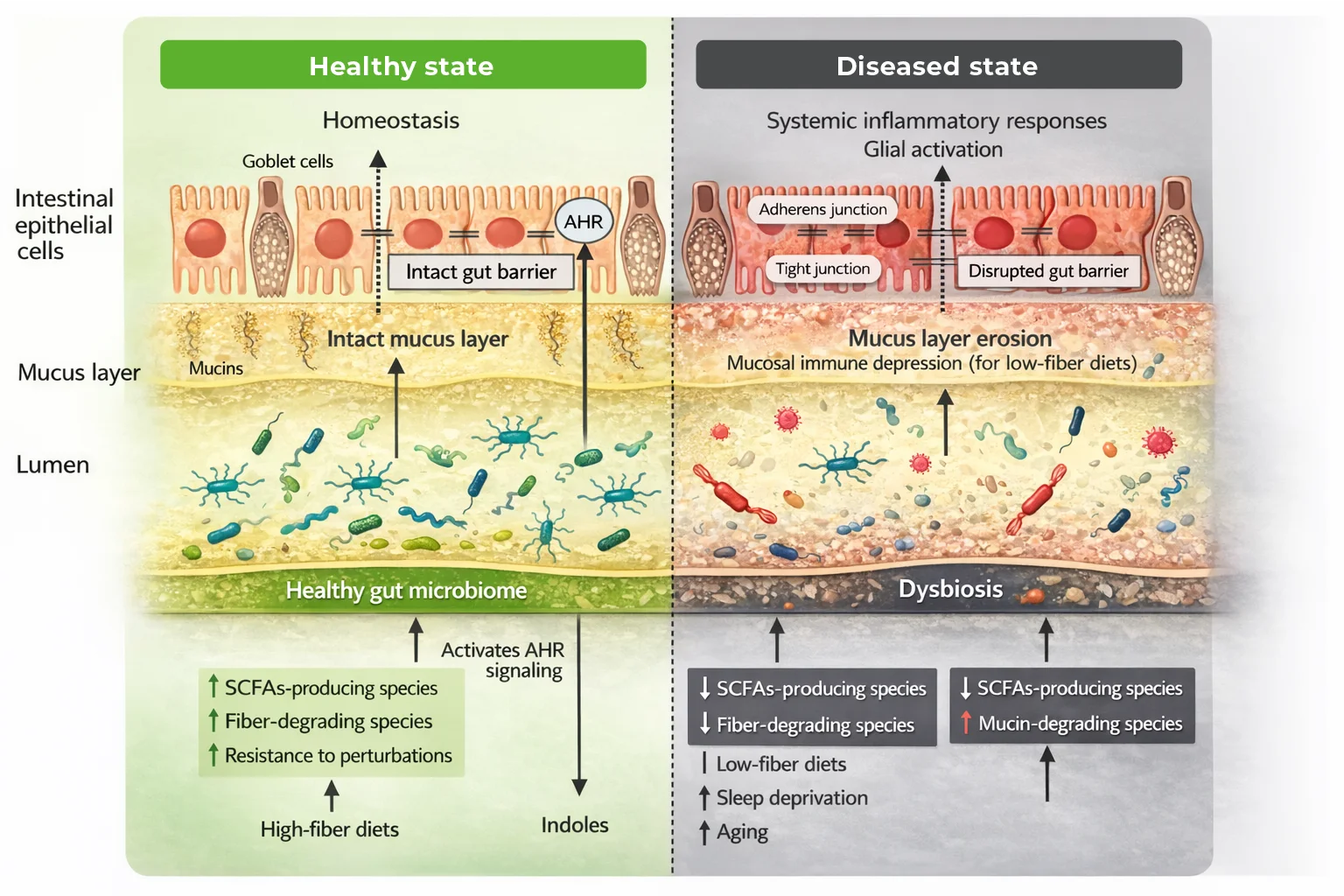
Hacer click sobre el cuadro para ampliar la imagen.
Loh JS, Mak WQ, Tan LKS, Ng CX, Chan HH, Yeow SH, Foo JB, Ong YS, How CW, Khaw KY. Microbiota-gut-brain axis and its therapeutic applications in neurodegenerative diseases. Signal Transduct Target Ther. 2024 Feb 16; 9(1):37. doi: 10.1038/s41392-024-01743-1. PMID: 38360862; PMCID: PMC10869798
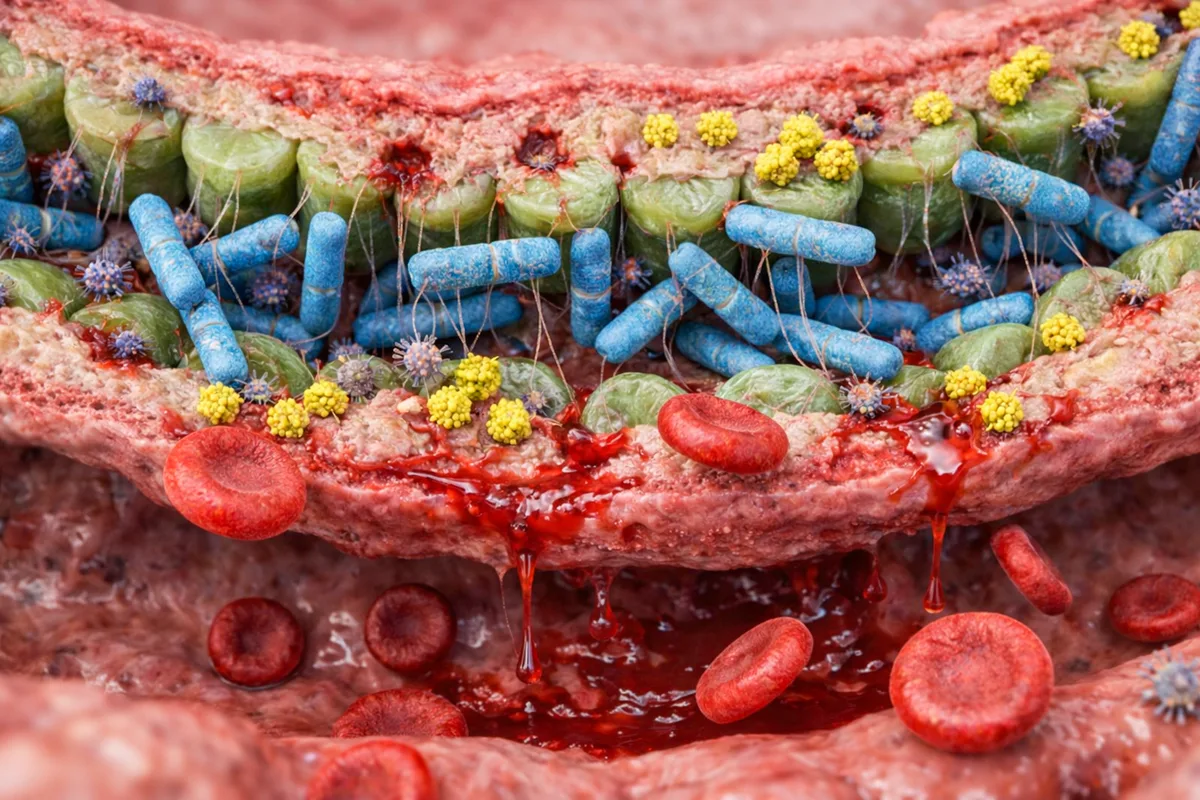
La microbiota intestinal funciona como un ecosistema dinámico cuya estabilidad depende de la cantidad y de la diversidad microbiana y particularmente de la producción de AGCC. Cuando este equilibrio se altera se instaura un estado de disbiosis caracterizado por la pérdida de bacterias beneficiosas y la reducción de metabolitos clave. Esto no solo compromete la integridad de la barrera intestinal, sino que favorece la permeabilidad y la translocación de componentes bacterianos además de la activación inflamatoria sistémica. Desde este punto de quiebre intestinal comienza a configurarse un terreno biológico propicio para el desarrollo de patologías metabólicas, inmunológicas y degenerativas de alta prevalencia.
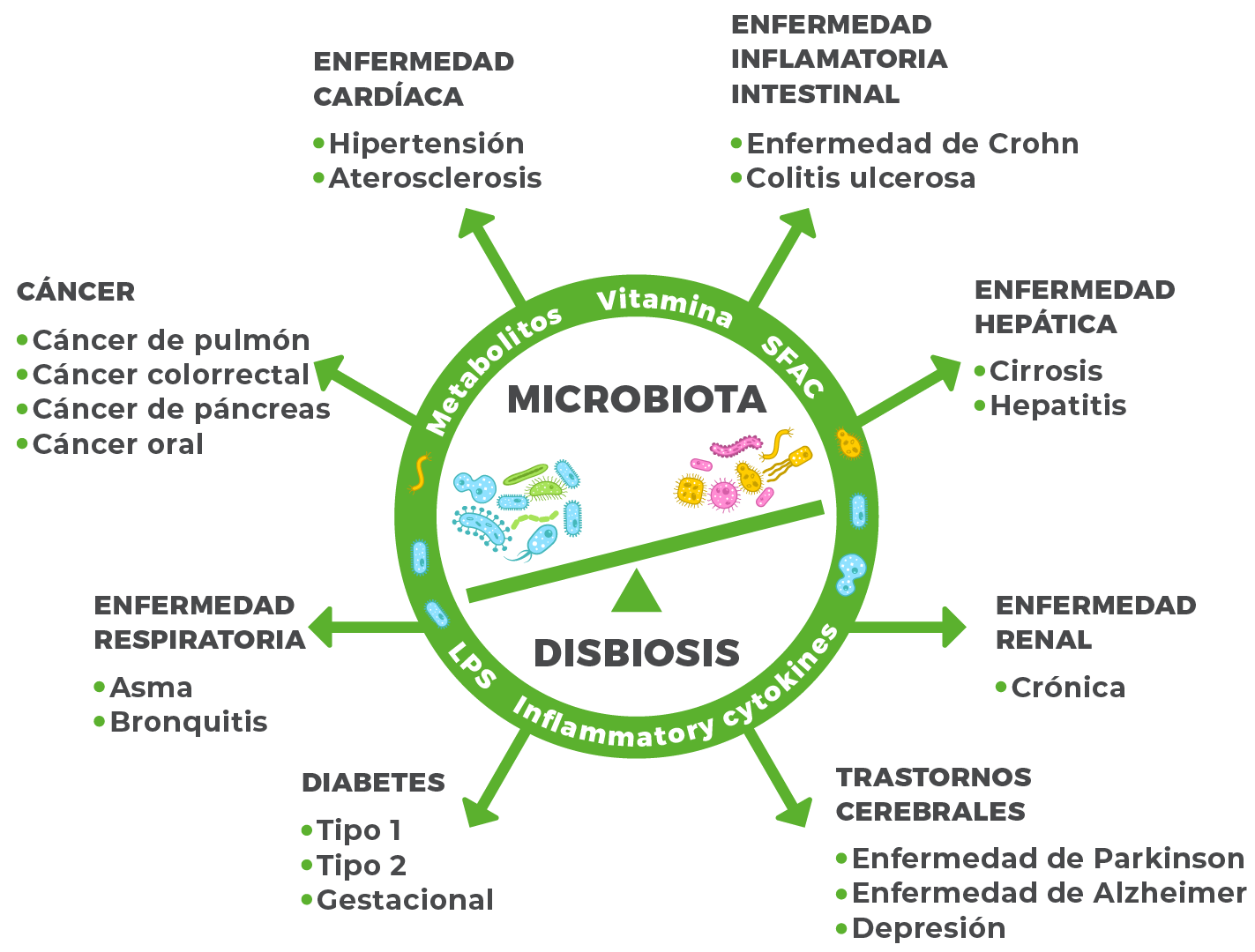
Hacer click sobre el cuadro para ampliar la imagen.
Hou K, Wu ZX, Chen XY, Wang JQ, Zhang D, Xiao C, Zhu D, Koya JB, Wei L, Li J, Chen ZS. Microbiota in health and diseases. Signal Transduct Target Ther. 2022 Apr 23;7(1):135. doi: 10.1038/s41392-022-00974-4. PMID: 35461318; PMCID: PMC9034083
Rol de los AGCC sobre el metabolismo

La disbiosis intestinal, caracterizada por la reducción de bacterias productoras de AGCC, favorece un entorno inflamatorio sistémico que impacta simultáneamente sobre la regulación metabólica y la función cardiovascular.
La reducción sostenida de estos metabolitos se asocia con el desarrollo y progresión de obesidad, diabetes tipo 2, dislipidemia, hígado graso, hipertensión, aterosclerosis y enfermedad cardiovascular, configurando un escenario en el que las alteraciones metabólicas y vasculares coexisten y se potencian recíprocamente.
Rol de los AGCC
Estimulan la secreción de péptidos incretínicos
Estimulan la secreción de péptidos incretínicos, como el Péptido similar al glucagón tipo 1 (GLP-1) que mejora la secreción de insulina dependiente de glucosa, enlentece el vaciamiento gástrico y reduce la glucemia postprandial, y el Péptido YY (PYY) que aumenta la saciedad y contribuye a reducir la ingesta calórica.
Modulan la gluconeogénesis hepática
Modulan la gluconeogénesis hepática, contribuyendo a regular la producción de glucosa en el hígado y favoreciendo el mantenimiento del equilibrio de los niveles de glucosa en sangre dentro de rangos fisiológicos.
Favorecen la oxidación de ácidos grasos
Favorecen la oxidación de ácidos grasos, lo que promueve un mejor uso de los ácidos grasos como fuente de energía, contribuyendo a un mayor equilibrio metabólico y a una menor acumulación de lípidos.
Regulan la lipólisis y el metabolismo del tejido adiposo
Regulan la lipólisis y el metabolismo del tejido adiposo, participando en el control de la liberación y el almacenamiento de ácidos grasos ayudando a mantener un balance energético adecuado.
Contribuyen a la regulación del colesterol
Contribuyen a la regulación del colesterol, favoreciendo su captación hepática desde el torrente sanguíneo y reduciendo sus niveles plasmáticos.
Cuando la producción de AGCC disminuye, este entramado regulatorio se altera, favoreciendo resistencia a la insulina, expansión del tejido adiposo inflamado, desregulación metabólica y amplificación del estado inflamatorio sistémico.
Impacto cardiovascular
El mismo entorno inflamatorio que condiciona el deterioro metabólico actúa sobre el sistema cardiovascular. La reducción sostenida de AGCC favorece la disfunción endotelial y la activación inflamatoria vascular, facilitando el deterioro progresivo y el aumento del riesgo cardiovascular.
Además, los AGCC ejercen funciones de señalización que influyen en la contractilidad miocárdica, la regulación de la presión arterial y la actividad del sistema nervioso autónomo. Su disminución puede alterar estos mecanismos de control, ampliando su repercusión sobre la función cardíaca y vascular.
Impacto en la función renal
Los AGCC desempeñan un papel central en el eje intestino–riñón, actuando como mediadores de protección renal. Contribuyen a reducir la inflamación, modular la presión arterial, fortalecer la barrera intestinal y limitar el pasaje de toxinas urémicas hacia la circulación sistémica. De este modo, atenúan la inflamación crónica de bajo grado y favorecen la preservación de la función renal.
En la enfermedad renal crónica, la acumulación de urea altera la microbiota intestinal y promueve un perfil disbiótico con disminución de bacterias productoras de AGCC. Esta alteración debilita la barrera intestinal y aumenta la permeabilidad, facilitando el pasaje de toxinas urémicas —como el indoxil sulfato y el TMAO— que promueven inflamación sistémica y aceleran el deterioro renal.
Los prebióticos, como la inulina, enriquecen selectivamente la microbiota incrementando bacterias productoras de AGCC. A través de este mecanismo, se favorece el refuerzo de la barrera intestinal y la modulación de la inflamación sistémica, disminuyen las toxinas urémicas y mejora la tasa de filtración glomerular.
Rol de AGCC en el sist. nervioso central
El intestino, la microbiota y el cerebro forman un sistema de comunicación bidireccional conocido como eje intestino–cerebro. Los AGCC actúan como mediadores clave en esta red, regulando la respuesta inmune, la integridad de las barreras biológicas y la función del sistema nervioso central.
Rol de los AGCC
Reducen la translocación de endotoxinas
En el intestino, refuerzan la estructura fisiológica de la mucosa al estimular la producción de mucina, fortalecen las uniones estrechas epiteliales y reducen la translocación de endotoxinas como los LPS cuya llegada al torrente sanguíneo puede promover neuroinflamación.
Protegen la barrera hemato encefálica (BHE)
Ejercen un efecto protector sobre la barrera hemato encefálica (BHE) reforzando su integridad, disminuyendo su permeabilidad y limitando la entrada de moléculas proinflamatorias al sistema nervioso central.
Modulan la actividad de la microglía
Modulan la actividad de la microglía, principales células inmunitarias innatas del sistema nervioso central, encargadas de funciones esenciales como la neurogénesis, la angiogénesis, la transmisión sináptica, la integridad de la mielina y la eliminación de neuronas apoptóticas y restos celulares. Cuando estas funciones se alteran, se favorece la progresión de procesos neurodegenerativos.
Reducen la neuroinflamación crónica
El butirato actúa como inhibidor de la histona deacetilasas (HDAC), enzima que regula la expresión génica mediante mecanismos epigenéticos. Al inhibir la HDAC, favorece una estructura más abierta de la cromatina, promoviendo la expresión de genes con funciones antiinflamatorias y neuroprotectoras. A través de este mecanismo, los AGCC contribuyen a reducir la neuroinflamación crónica de bajo grado y a sostener un entorno cerebral más favorable para la memoria y el aprendizaje.
Impacto en las enfermedades neurodegenerativas

La endotoxina LPS, componente de la pared de bacterias Gram negativas favorece la agregación del péptido β-amiloide (Aβ), derivado de la proteína precursora amiloide, capaz de atravesar tanto la barrera intestinal como la BHE. La disbiosis intestinal y el aumento de la permeabilidad intestinal facilitan el pasaje de LPS a la circulación sistémica, activando el sistema inmune periférico, potenciando la neuroinflamación y favoreciendo el depósito de proteínas amiloides en el sistema nervioso central, contribuyendo a la patogénesis de la enfermedad de Alzheimer.
Más de 50 metabolitos microbianos se han asociado positivamente con un deterioro cognitivo acelerado y con una edad de inicio más temprana. Entre estos metabolitos se encuentra el óxido de trimetilamina-N (TMAO), derivado del metabolismo microbiano de las grasas animales de la dieta. Se ha demostrado que el TMAO está presente en el sistema nervioso central humano, lo que refuerza la evidencia de que los metabolitos microbianos migran hacia el cerebro.
El impacto sistémico y neurológico de estos metabolitos depende en gran medida de la integridad de la barrera intestinal. En condiciones fisiológicas de eubiosis, una barrera intestinal funcional limita su paso a la circulación sistémica. Por el contrario, la alteración de la permeabilidad intestinal facilita la translocación de metabolitos como el TMAO, permitiendo su llegada al sistema nervioso central, contribuyendo a la patogénesis de la enfermedad de Alzheimer.
En la enfermedad de Parkinson, la disbiosis intestinal también desempeña un papel central. El aumento de bacterias Gram negativas, la mayor liberación de LPS y la permeabilidad intestinal favorecen inflamación crónica y estrés oxidativo, condiciones que promueven el mal plegamiento y la agregación de la α-sinucleína en el sistema nervioso entérico. Esta proteína patológica puede propagarse hacia el cerebro a través del nervio vago y diseminarse progresivamente, afectando especialmente a las neuronas dopaminérgicas de la sustancia negra. Este proceso se asocia con activación microglial persistente, alteración de la BHE y progresión tanto de los síntomas motores (bradicinesia, rigidez, temblor) como de manifestaciones no motoras, incluyendo trastornos gastrointestinales y deterioro cognitivo.

Tanto en Alzheimer como en Parkinson se ha observado una reducción de bacterias productoras de butirato y menores concentraciones de AGCC asociadas con mayor activación microglial, alteración de la BHE y progresión del daño sináptico. Dado que los AGCC modulan la expresión génica y limitan la activación inflamatoria, su disminución no solo refleja disbiosis, sino la pérdida de un regulador fundamental de la estabilidad cerebral y un punto crítico en la evolución de las enfermedades neurodegenerativas. Asimismo, niveles reducidos de AGCC se han vinculado con trastornos del estado de ánimo, particularmente depresión, donde la inflamación sistémica de bajo grado y la disfunción de la BHE desempeñan un papel relevante.
Rol de los AGCC sobre el sistema inmune
En las patologías inmunológicas, la disbiosis intestinal favorece la instauración de un estado inflamatorio persistente que compromete la homeostasis sistémica. La disminución de los AGCC debilita los mecanismos de regulación de la respuesta inmune y altera la integridad de la barrera intestinal, promoviendo un perfil proinflamatorio sostenido.
La mayor permeabilidad intestinal facilita la translocación de componentes bacterianos, especialmente de LPS hacia el torrente sanguíneo. Éstos son reconocidos por receptores de la inmunidad innata, activando cascadas de señalización intracelular que inducen la transcripción y liberación de citoquinas proinflamatorias. Esta activación sostenida incrementa el estrés oxidativo y perpetúa un estado de inflamación crónica de bajo grado que puede afectar órganos distante.
Rol de los AGCC
Mantienen la barrera intestinal
Contribuyen al mantenimiento de la barrera intestinal. Favorecen la producción de mucina y el fortalecimiento de la capa de moco que recubre el epitelio, reforzando la integridad estructural de la mucosa. Al preservar esta barrera física y funcional, disminuyen la permeabilidad intestinal y limitan la activación inmunológica secundaria a la translocación microbiana.
Modulan la respuesta inmunitaria intestinal y sistémica
Modulan la respuesta inmunitaria intestinal y sistémica. Los AGCC ayudan a mantener un equilibrio entre activación y control de la inflamación. Favorecen una respuesta eficaz frente a estímulos sin que esta se vuelva excesiva o persistente, evitando el daño asociado a la inflamación crónica.
Ejercen un efecto inmunomodulador sistémico
Promueven un perfil antiinflamatorio, estimulando la producción de citoquinas con efecto antiinflamatorio reduciendo la expresión de citoquinas proinflamatorias. Ejercen un efecto inmunomodulador sistémico. Su acción reguladora sobre el perfil inflamatorio se extiende más allá del intestino, influyendo en la respuesta inmune en distintos tejidos.
Limitan la inflamación crónica
Regulan la expresión génica mediante mecanismos epigenéticos. El butirato y en menor medida otros AGCC actúan como inhibidor de HDAC, modulando la estructura de la cromatina y favoreciendo la expresión de genes con funciones antiinflamatorias, antiproliferativas y proapoptóticas. Este mecanismo contribuye a limitar la inflamación crónica y se asocia con potenciales efectos anticarcinogénicos y antitumorales.
En las patologías inmunológicas, los AGCC cumplen un papel decisivo como moduladores de la respuesta inflamatoria. Su capacidad para equilibrar la producción de citoquinas, preservar la integridad de la barrera intestinal y limitar el aumento de la permeabilidad —reduciendo así la translocación microbiana y la activación inmune sostenida— los convierte en elementos clave para el mantenimiento de la homeostasis inmunológica.
Cuando su producción disminuye, se debilita la barrera epitelial, aumenta la permeabilidad intestinal y se perpetúa la activación inflamatoria. Este escenario favorece la progresión de enfermedades inflamatorias intestinales y respiratorias (asma), así como la generación de un microambiente propicio para alteraciones celulares asociadas al desarrollo tumoral. De este modo, los AGCC se consolidan como metabolitos reguladores clave de los procesos inmunológicos vinculados a inflamación crónica.
Estrategias para aumentar la producción de AGCC
prebióticos
Los prebióticos son fibras fermentables selectivamente que modulan la composición y la actividad de la microbiota intestinal, promoviendo un entorno microbiano más favorable y aumentando la producción de AGCC.
Diferencia entre fibra dietética y fibra dietética PREBIÓTICA
La fibra se define como polímeros de carbohidratos que contienen ≥ 10 unidades monoméricas que resisten la digestión por enzimas endógenas en el intestino delgado. La fibra se puede dividir en soluble e insoluble.
Aunque todos los prebióticos son fibra, no toda la fibra es prebiótica.
Para que una fibra se considere prebiótica debe cumplir con las siguientes características:
Resistente
Resistir la acidez gástrica e hidrólisis enzimática (no es afectado por enzimas presentes en la saliva, así como enzimas pancreáticas e intestinales) y la absorción en el tracto gastrointestinal superior.
Estimulante
Estimular selectivamente el crecimiento y/o la actividad de las bacterias intestinales benéficas que contribuyen a la salud y bienestar.
Fermentado
Debe ser fermentada por la microbiota intestinal.
FIBRA INSOLUBLE
FIBRA SOLUBLE
FIBRA PREBIÓTICA
Celulosa.
Psyllium.
Inulina, Fructooligosacáridos, Galactooligosacáridos.
La inulina es una de las fibras solubles prebióticas más estudiadas y reconocidas. Se caracteriza por su efecto bifidogénico, ya que estimula selectivamente el crecimiento de Bifidobacterias, y su fermentación colónica da lugar a la producción de AGCC.
Beneficios de la INULINA sobre la salud
Enriquece de la microbiota intestinal
La inulina llega intacta al colon y es fermentada sobre todo por las especies de los géneros Bifidobacterium y Lactobacillus, lo que incrementa su abundancia. Además, las Bifidobacterias y Lactobacilos compiten por nutrientes y sitios de adhesión en la mucosa, limitando el espacio disponible para patógenos y reduciendo así su proliferación. De esta manera, la inulina contribuye a un ecosistema intestinal equilibrado y protector.
Mejora el tránsito intestinal, reduce el estreñimiento y mejora la consistencia de las heces
Los AGCC estimulan la motilidad intestinal. La fermentación de la inulina aumenta la biomasa bacteriana, lo que incrementa el volumen de las heces. Además, la inulina retiene agua, favoreciendo heces más blandas y fáciles de evacuar. En conjunto, mejora el tránsito gastrointestinal y la regularidad intestinal.
Produce AGCC: acetato, butirato y propionato
La fermentación de la inulina por las bacterias intestinales produce como metabolitos principales a los AGCC que son los principales mediadores de los efectos beneficiosos de la inulina. Estos metabolitos mejoran la barrera intestinal al reforzar las uniones estrechas y reducir la permeabilidad intestinal. Los AGCC bajan el pH intestinal, creando un ambiente menos favorable para microorganismos patógenos. Los AGCC además estimulan la motilidad intestinal y tienen acción antiinflamatoria al regular la expresión de citoquinas proinflamatorias. A nivel sistémico actúan sobre el equilibrio metabólico de la glucosa y de los lípidos.
Mejora la absorción de nutrientes especialmente los minerales claves para la salud ósea
Los AGCC producidos durante la fermentación de la inulina bajan el pH del lumen intestinal, lo que aumenta la solubilidad de minerales como el calcio, magnesio y el hierro, facilitando su absorción. La suplementación con inulina ha demostrado que aumenta la absorción intestinal del calcio y del magnesio, nutrientes claves para la salud ósea, especialmente relevantes en mujeres postmenopáusicas y otras poblaciones con mayores requerimientos. Estudios clínicos demostraron un aumento en la absorción de calcio cuando se utilizaron suplementos con inulina.
Mejora los parámetros antropométricos
La inulina, al no ser digerible, retrasa el vaciado gástrico aumentando la secreción de hormonas de la saciedad, mejorando los parámetros antropométricos.
Los estudios han demostrado que, a dosis altas administradas durante un período prolongado, se produce un aumento de Bifidobacterias que se asocia con mejoras en estos valores, especialmente en el peso corporal e índice de masa corporal.
Los AGCC desempeñan un papel crucial en el metabolismo energético, mediante su participación en diferentes vías ayudan a regular el apetito.
Aumenta el metabolismo de la glucosa, reduciendo los niveles de insulina
La inulina retrasa la absorción de glucosa en el intestino, ayudando a regular el aumento de los niveles de glucosa en sangre después de las comidas, favoreciendo la homeostasis glucémica.
El efecto bifidogénico se ha asociado con una mayor sensibilidad a la insulina y mejores niveles de insulina en sangre. El propionato, butirato y especialmente el acetato activan los receptores de las células beta-pancreáticas, regulando la secreción de insulina y mejorando la homeostasis de la glucosa.
Efectos favorables en la Enfermedad renal crónica
En la enfermedad renal crónica, la acumulación de urea altera la microbiota intestinal y aumenta la permeabilidad de la barrera epitelial, favoreciendo la entrada de toxinas urémicas como el sulfato de indoxilo, p-cresol y TMAO, compuestos que promueven endotoxemia e inflamación sistémica.
La modificación de la microbiota mediante prebióticos como la inulina se plantea como una estrategia terapéutica complementaria para reducir la producción de toxinas urémicas de origen intestinal y la inflamación.
Estudios clínicos han demostrado que la suplementación con inulina puede:
Modificar favorablemente la composición de la microbiota intestinal.
Reducir los niveles séricos de ácido úrico y aumentar su degradación fecal en pacientes con insuficiencia renal.
Limitar la producción de indoles en pacientes sometidos a diálisis peritoneal.
Disminuir los niveles séricos de sulfato de indoxilo.
Mejorar la tasa de filtración glomerular.
Reducir los niveles de proteína C reactiva de alta sensibilidad.
Efectos beneficiosos sobre la inflamación y función inmune
Los estudios muestran que la inulina aumenta significativamente diferentes especies de Bifidobacterias, destacando B. Longum, B. Teenageis y B. Angulatum. Las bifidobacterias tienen efectos bien documentados sobre la modulación de la inflamación y la reducción de marcadores inflamatorios, tanto a nivel intestinal como sistémico:
Disminución de citoquinas proinflamatorias como TNF-α, IL-6, IL-1β.
Aumento de citoquinas antiinflamatorias como IL-10.
Reducción de la proteína C reactiva (PCR), un marcador inflamatorio sistémico.
La inulina al disminuir el pH del colon y mejorar la biomasa de la microbiota obstaculiza y previene el desarrollo de especies patógenas, reduciendo significativamente el número de poblaciones de especies pertenecientes al género Clostridium lo que conduce a una reducción de la inflamación y a una mejor salud digestiva general y absorción de nutrientes.
Impacto positivo en el perfil lipídico
La inulina puede interferir en la absorción de la grasa dietética y el colesterol ayudando a disminuir los niveles de sangre de la lipoproteína de baja densidad (LDL).
A diferentes dosis la inulina puede reducir los niveles de colesterol total, LDL y triglicéridos en sangre dado que los AGCC pueden regular la lipogénesis mediante diferentes mecanismos.
Además, es capaz de aumentar los niveles séricos de la lipoproteína de alta densidad (HDL) cuando se administra durante un prolongado periodo de tiempo.
probióticos
Los probióticos son microorganismos vivos reconocidos como habitantes normales del intestino humano que, al ser ingeridos, modulan la microbiota y favorecen la fermentación de sustratos no digeribles, contribuyendo al aumento en la producción de AGCC. Si bien los AGCC representan uno de los principales mecanismos mediante los cuales la microbiota ejerce efectos, los probióticos también aportan beneficios independientes, incluyendo la modulación directa del sistema inmune, la competencia con patógenos, la producción de metabolitos bioactivos y la regulación de la función de barrera intestinal.
Los probióticos deben administrarse en cantidades adecuadas: se recomienda diariamente al menos mil millones de unidades formadoras de colonias (UFC) y deben contar con la identificación precisa a nivel género/ especie/ subespecie ya que sus efectos son cepa-dependientes. Cuando se emplean cepas correctamente identificadas y en concentraciones apropiadas, su consumo se considera seguro.
Conclusión
Los AGCC ya no pueden entenderse como simples subproductos de la fermentación bacteriana. Son verdaderos metabolitos biológicos que articulan la comunicación entre microbiota y organismo, regulando procesos metabólicos, inmunológicos y estructurales que sostienen la salud sistémica.
Cuando su producción se preserva, contribuyen al equilibrio energético, a la integridad de las barreras biológicas y al control de la inflamación, manteniendo un entorno estable y funcional. Pero cuando la disbiosis reduce su disponibilidad, se rompe un delicado sistema de regulación: disminuye la integridad de la barrera intestinal, aumenta la permeabilidad, se facilita el pasaje de componentes microbianos hacia la circulación (LPS), emerge la inflamación crónica de bajo grado, se altera el metabolismo, se debilitan los mecanismos inmunológicos y se favorecen procesos degenerativos.
Desde el intestino se proyecta así una pérdida progresiva de integridad estructural y funcional, en la que el aumento de la permeabilidad actúa como punto de inflexión entre la alteración local de la microbiota y sus consecuencias sistémicas. Comprender el rol de los AGCC permite integrar bajo un mismo marco fisiopatológico alteraciones metabólicas, inmunológicas y degenerativas, revelando que múltiples enfermedades crónicas comparten un origen común en la pérdida de homeostasis mediada por la disbiosis y la disminución de sus metabolitos reguladores.
En definitiva, el intestino no es solo un órgano digestivo, sino un centro regulador sistémico. Los AGCC, lejos de ser simples metabolitos, son piezas clave en el delicado equilibrio entre salud y enfermedad.
Comprender el rol de los AGCC permite integrar múltiples alteraciones metabólicas, inmunológicas y degenerativas bajo un mismo marco fisiopatológico. No obstante, la modulación de la microbiota a través de prebióticos y probióticos trasciende la producción de AGCC, involucrando mecanismos inmunológicos, estructurales y moleculares independientes que amplían su impacto biológico. De este modo, preservar la homeostasis microbiana implica conservar tanto la producción de AGCC como las múltiples funciones regulatorias independientes de la microbiota, cuya alteración contribuye al desarrollo de enfermedades crónicas.
Fuentes
Vacca A, Brosolo G, Marcante S, Della Mora S, Bulfone L, Da Porto A, Pagano C, Catena C, Sechi LA. Gut Microbiota and Short-Chain Fatty Acids in Cardiometabolic HFpEF: Mechanistic Pathways and Nutritional Therapeutic Perspectives. Nutrients. 2026; 18(2):321. https://doi.org/10.3390/nu18020321
Alonso-Allende J, Milagro FI, Aranaz P. Health Effects and Mechanisms of Inulin Action in Human Metabolism. Nutrients. 2024 Sep 2; 16(17):2935. doi: 10.3390/nu16172935. PMID: 39275251; PMCID: PMC11397174.
Reyes Díaz RA, Cruz Lara NM. Papel de la microbiota intestinal en el desarrollo del síndrome metabólico: revisión narrativa. Revista De Nutrición Clínica y Metabolismo. 2024; 7(1):45–54. doi: 10.35454/rncm.v7n1.551
Loh, J.S., Mak, W.Q., Tan, L.K.S. y otros. Eje microbiota–intestino–cerebro y sus aplicaciones terapéuticas en enfermedades neurodegenerativas. Objetivo de transducción de siglas Ther 9, 37 (2024). https://doi.org/10.1038/s41392-024-01743-1
Birkeland E, Gharagozlian S, Valeur J, Aas AM. Short-chain fatty acids as a link between diet and cardiometabolic risk: a narrative review. Lipids Health Dis. 2023 Mar 14;22(1):40. doi: 10.1186/s12944-023-01803-5. PMID: 36915164; PMCID: PMC10012717
Fusco W, Lorenzo MB, Cintoni M, Porcari S, Rinninella E, Kaitsas F, Lener E, Mele MC, Gasbarrini A, Collado MC, et al. Short-Chain Fatty-Acid-Producing Bacteria: Key Components of the Human Gut Microbiota. Nutrients. 2023; 15(9):2211. https://doi.org/10.3390/nu15092211
Hou K, Wu ZX, Chen XY, Wang JQ, Zhang D, Xiao C, Zhu D, Koya JB, Wei L, Li J, Chen ZS. Microbiota in health and diseases. Signal Transduct Target Ther. 2022 Apr 23;7(1):135. doi: 10.1038/s41392-022-00974-4. PMID: 35461318; PMCID: PMC9034083.
Dalile B, Van Oudenhove L, Vervliet B, Verbeke K. The role of short-chain fatty acids in microbiota–gut–brain communication. Nat Rev Gastroenterol Hepatol. 2019; 16(8):461–478. doi: 10.1038/s41575-019-0157-3