Enfermedades neurodegenerativas
Las enfermedades neurodegenerativas constituyen un grupo heterogéneo de trastornos crónicos y progresivos que afectan al sistema nervioso central y/o periférico, caracterizados por la pérdida gradual y selectiva de neuronas que conducen al deterioro de sus funciones. Entre las enfermedades neurodegenerativas más prevalentes se incluyen: enfermedad de Alzheimer y enfermedad de Parkinson.
A pesar de las diferencias en la presentación clínica ambas patologías presentan características comunes como neurodegeneración progresiva, deterioro cognitivo y disminución de la función motora. La etiología de estos trastornos sigue siendo compleja y multifactorial, involucrando una combinación de factores genéticos y ambientales.
Hallazgos recientes indican que la microbiota intestinal desempeña un papel clave en la fisiopatología y el desarrollo de los trastornos neurodegenerativos.
Mecanismos de Señalización del Eje Microbiota – Intestino – Cerebro
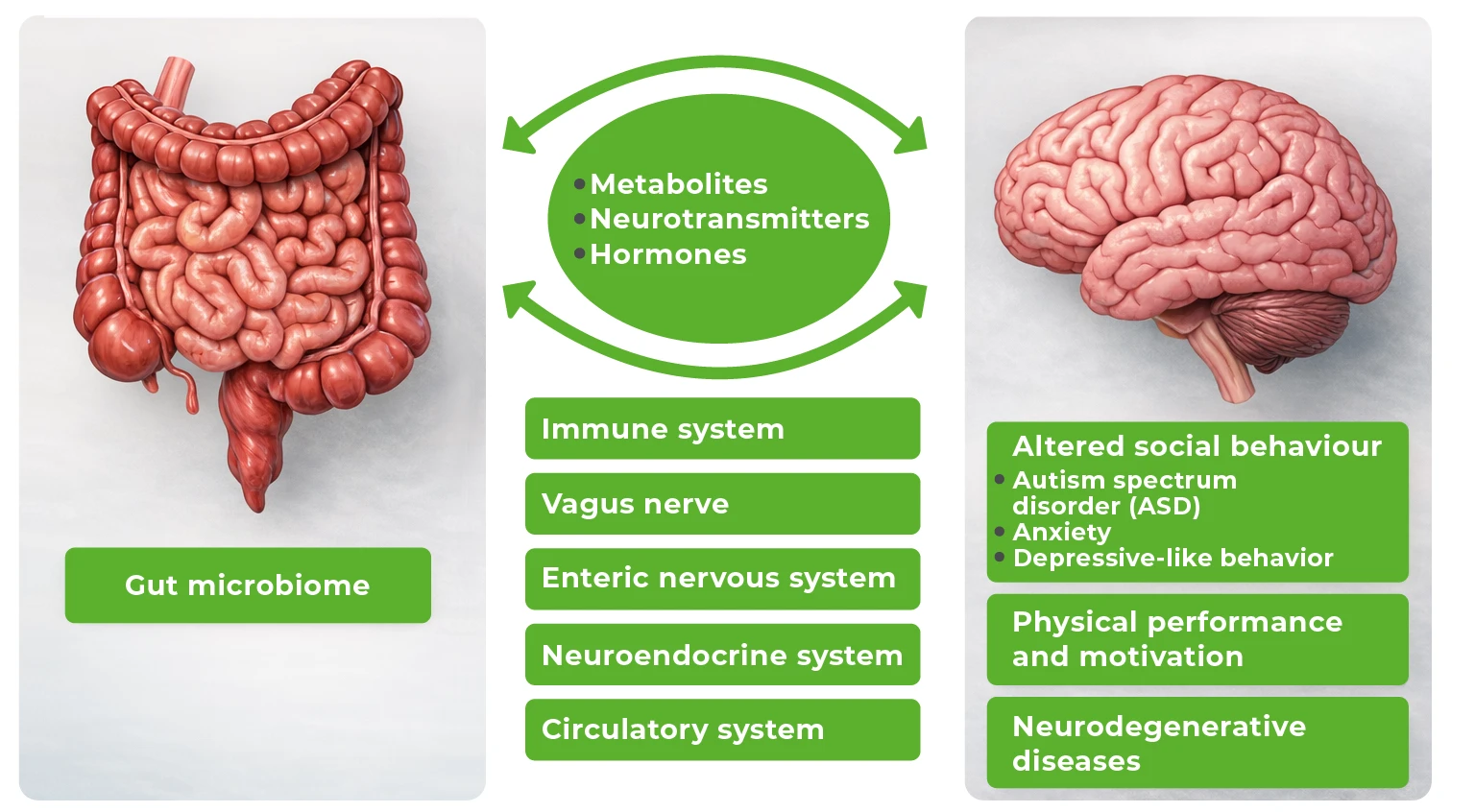
El intestino, la microbiota intestinal y el cerebro forman un sistema interconectado de procesos y comunicación conocido como eje intestino-cerebro-microbiota. Este sistema complejo implica una señalización bidireccional de metabolitos, neurotransmisores y hormonas a través de varias vías: sistema inmunitario, nervio vago, sistema neuroendócrino y sistema circulatorio.
Microbiota gut-brain axis
Hacer click sobre el cuadro para ampliar la imagen.
Figura 1. El eje microbiota-intestino-cerebro. La comunicación bidireccional entre la microbiota intestinal y el cerebro está mediada por el sistema inmunitario, el nervio vago, el sistema nervioso entérico, el sistema neuroendócrino y el sistema circulatorio.
Loh, J.S., Mak, W.Q., Tan, L.K.S. y otros. Eje microbiota–intestino–cerebro y sus aplicaciones terapéuticas en enfermedades neurodegenerativas. Objetivo de transducción de siglas Ther 9, 37 (2024). https://doi.org/10.1038/s41392-024-01743-1
En los últimos años, la evidencia ha señalado que estos procesos neurodegenerativos se encuentran estrechamente vinculados a alteraciones de la microbiota intestinal, las cuales pueden modular mecanismos clave como la neuroinflamación y la permeabilidad de barreras biológicas.
El rol central de los ácidos grasos de cadena corta
Integridad de la barrera intestinal y hematoencefálica
Mantenimiento de la integridad de las barreras intestinal y hematoencefálica (BHE)
Los ácidos grasos de cadena corta (AGCC) -principalmente acetato, propionato y butirato- producidos por la fermentación de fibras prebióticas como la INULINA desempeñan un papel central en el mantenimiento de la integridad de las barreras intestinal y hematoencefálica (BHE). En el intestino, refuerzan la estructura fisiológica de la mucosa al estimular la producción de mucina, fortalecer las uniones estrechas epiteliales y reducir la traslocación de endotoxinas como los lipopolisacáridos (LPS), cuya llegada al torrente sanguíneo puede promover neuroinflamación. De forma complementaria, los AGCC ejercen un efecto protector sobre la BHE, disminuyendo su permeabilidad y limitando la entrada de moléculas proinflamatorias al sistema nervioso central.
Influir en la composición y estabilidad de la microbiota
La capa de moco intestinal constituye la primera línea de defensa de esta barrera. Es una estructura dinámica y parcialmente permeable compuesta principalmente por mucinas, proteínas altamente glicosiladas secretadas por las células caliciformes. Además de su función física, esta capa modula la inmunidad local al influir en la composición y estabilidad de la microbiota. Con el envejecimiento, la integridad de la barrera intestinal se deteriora gradualmente, lo que facilita la translocación al torrente sanguíneo de metabolitos proinflamatorios y productos bacterianos patógenos. Esta mayor permeabilidad intestinal amplifica la inflamación sistémica y contribuye al debilitamiento de la BHE, favoreciendo la neuroinflamación y la progresión neurodegenerativa.
Preservar la integridad de la capa de moco
Los AGCC resultan fundamentales para preservar la integridad de la capa de moco. Una ingesta elevada de fibra prebiótica promueve el crecimiento de bacterias productoras de AGCC, estimula la secreción de mucina y favorece una microbiota más estable y resiliente. Por el contrario, dietas bajas en fibra facilitan la expansión de bacterias degradadoras de mucina, erosionan la capa de moco y aumentan la susceptibilidad a patógenos, lo que conduce a respuestas inmunes alteradas que culminan en inflamación sistémica, neuroinflamación y neurodegeneración. Además de los AGCC, otros metabolitos microbianos, como el indol y sus derivados procedentes del triptófano dietario, también contribuyen al mantenimiento de la barrera intestinal al fortalecer el complejo de uniones epiteliales y modular vías inmunológicas claves.
Hacer click sobre el cuadro para ampliar la imagen.
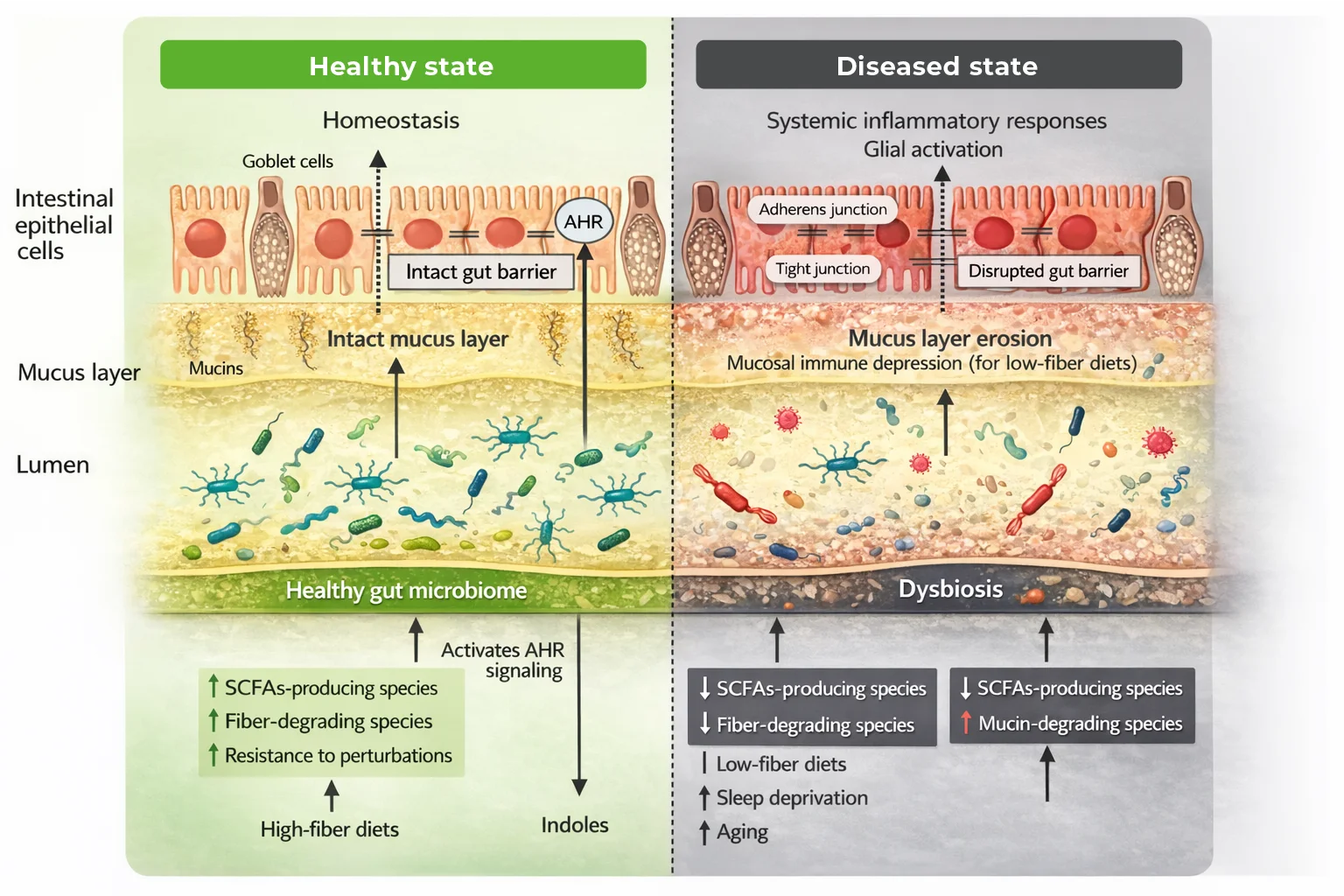
Figura 2. Eje microbiota-intestino-cerebro. a Las dietas ricas en fibra contribuyen a un microbioma intestinal saludable y mejoran la integridad de la barrera intestinal al aumentar las especies productoras de AGCC. El indol y sus derivados mejoran la integridad de la barrera intestinal al activar los receptores de hidrocarburos arílicos (AHR) epiteliales. b Las dietas bajas en fibra, el envejecimiento y la falta de sueño contribuyen a la disbiosis y alteran la integridad de la barrera intestinal al reducir las especies productoras de AGCC y las que degradan la fibra y la mucina. Las dietas bajas en fibra inducen inmunodepresión mucosa y sistémica.
Loh, J.S., Mak, W.Q., Tan, L.K.S. y otros. Eje microbiota–intestino–cerebro y sus aplicaciones terapéuticas en enfermedades neurodegenerativas. Objetivo de transducción de siglas Ther 9, 37 (2024). https://doi.org/10.1038/s41392-024-01743-1
Neuroinflamación crónica de bajo grado
Modulan la microglía influyendo en su maduración y activación
Los AGCC modulan la actividad de la microglía, principales células inmunitarias innatas del sistema nervioso central, encargadas de funciones esenciales como la neurogénesis, la angiogénesis, la transmisión sináptica, la integridad de la mielina y la eliminación de neuronas apoptóticas y restos celulares. Cuando estas funciones se alteran, se favorece la progresión de procesos neurodegenerativos. Un rol central de la microglía es el reconocimiento y la depuración eficiente de agregados proteicos y desechos celulares sin dañar el tejido circundante, preservando la homeostasis cerebral. Sin embargo, durante el envejecimiento y en las enfermedades neurodegenerativas, su capacidad fagocítica se vuelve menos eficaz, lo que conduce a la acumulación de compuestos tóxicos y a la liberación sostenida de citoquinas proinflamatorias. Esta activación crónica genera una neuroinflamación persistente de bajo grado que resulta perjudicial para las neuronas y las sinapsis, promoviendo la neurodegeneración y el deterioro cognitivo. Los AGCC modulan la microglía influyendo en su maduración y activación.
Mejorar la función
neurocognitiva
El butirato es un potente inhibidor de las histona deacetilasa (HDAC), favoreciendo la expresión de genes antiinflamatorios y neuroprotectores. La HDAC es una enzima que regula la expresión génica mediante mecanismos epigenéticos al eliminar grupos acetilo de las histonas, proteínas alrededor de las cuales se enrolla el ADN formando la cromatina. Cuando las histonas se encuentran acetiladas, la cromatina adopta una conformación más abierta que favorece la transcripción génica. Cuando la HDAC remueve estos grupos acetilo, induce la condensación de la cromatina y reduce o silencia la expresión de determinados genes. La producción de AGCC a través de la dieta o de una microbiota saludable puede mejorar la función neurocognitiva, y uno de los mecanismos clave es la inhibición de HDAC especialmente por el butirato. Este mecanismo contribuye a mantener la microglía en un estado homeostático, reduciendo la neuroinflamación crónica de bajo grado, lo que crea un entorno cerebral más favorable para procesos cognitivos como la memoria y el aprendizaje.

Enfermedad de Alzheimer
La enfermedad de Alzheimer es un trastorno neurodegenerativo progresivo y la causa más común de demencia, que afecta a más de 50 millones de personas en todo el mundo, con proyecciones que indican que esta cifra podría triplicarse para el año 2050.
Los síntomas clínicos de la enfermedad de Alzheimer incluyen un deterioro progresivo de la cognición, la memoria y las capacidades funcionales, así como alteraciones en el comportamiento y el temperamento. Estos síntomas se han atribuido en gran medida a la manifestación de dos marcadores patológicos característicos: las placas extracelulares de beta-amiloide (Aβ) y los ovillos neurofibrilares intracelulares (NFTs). La endotoxina LPS, componente de la pared de bacterias Gram negativas como Escherichia coli, favorece la agregación del Aβ, un péptido derivado de la proteína precursora amiloide capaz de atravesar tanto la barrera intestinal como la BHE, incrementando la carga amiloide observada en los cerebros con enfermedad de Alzheimer. La disbiosis intestinal y la alteración de la barrera intestinal, conocida como “intestino permeable”, aumentan la liberación de este LPS hacia la circulación sistémica, lo que contribuye a la activación del sistema inmune periférico, potencia las respuestas neuroinflamatorias y facilita el depósito de proteínas amiloides microbianas producidas periféricamente en el sistema nervioso central, promoviendo así la patogénesis de la enfermedad de Alzheimer.
Más de 50 metabolitos microbianos se han asociado positivamente con un deterioro cognitivo acelerado y con una edad de inicio más temprana. Entre estos metabolitos se encuentra el óxido de trimetilamina-N (TMAO), derivado del metabolismo microbiano de las grasas animales de la dieta. La asociación del TMAO con la enfermedad de Alzheimer respalda hallazgos epidemiológicos que indican que las dietas occidentales ricas en grasas se correlacionan positivamente con un mayor riesgo de desarrollar esta patología. Se ha demostrado que el TMAO está presente en el sistema nervioso central humano, lo que refuerza la evidencia de que los metabolitos microbianos migran hacia el cerebro. El impacto sistémico y neurológico de estos metabolitos depende en gran medida de la integridad de la barrera intestinal. En condiciones fisiológicas de eubiosis, una barrera intestinal funcional limita su paso a la circulación sistémica. Por el contrario, la alteración de la permeabilidad intestinal facilita la translocación de metabolitos como el TMAO, permitiendo su llegada al sistema nervioso central, contribuyendo a la patogénesis de la enfermedad de Alzheimer.
Marcadores metabólicos distintos de un mismo contexto de disbiosis intestinal
Desde una perspectiva funcional, la TMAO y la endotoxina LPS pueden entenderse como marcadores metabólicos distintos de un mismo contexto de disbiosis intestinal. Un perfil de microbiota con elevada capacidad de producción de TMAO plasmático suele coexistir con una mayor abundancia relativa de bacterias Gram negativas, lo que se asocia a un incremento en la liberación de LPS y una mayor permeabilidad intestinal.
Regula la integridad de la barrera epitelial intestinal
La microbiota intestinal regula la integridad de la barrera epitelial intestinal. La presencia de bacterias comensales, como Lactobacillus rhamnosus, protege frente al aumento de la permeabilidad intestinal al incrementar la expresión colónica de proteínas de unión estrecha como la ocludina y la (E)-cadherina epitelial. Además la microbiota intestinal modula la expresión de proteínas de unión estrecha de la BHE a través de los AGCC.
Regulación de la neuroinflamación y la homeostasis metabólica
La disbiosis intestinal y la disminución de los metabolitos microbianos, como los AGCC contribuyen a la disfunción de la BHE, la inflamación crónica y el deterioro sináptico. Los AGCC, en particular el butirato, desempeñan un papel clave en la regulación de la neuroinflamación y la homeostasis metabólica. En la enfermedad de Alzheimer se observa una disminución de bacterias productoras de butirato, lo que debilita las defensas antiinflamatorias y favorece la neuroinflamación.
En síntesis, la microbiota intestinal regula la función inmunitaria, la integridad de las barreras intestinal y BHE y los procesos neuroinflamatorios. Los AGCC, especialmente el butirato, desempeña un rol central en el eje intestino–cerebro al regular las respuestas inmunitarias, reforzar la integridad de la BHE y limitar los procesos neuroinflamatorios. La reducción significativa de estos metabolitos en sangre y heces observada en la enfermedad de Alzheimer se asocia estrechamente con el deterioro cognitivo y el aumento de la neuroinflamación.
La incorporación de fibra prebiótica como la INULINA que favorece la producción de AGCC, y probióticos como el Lactobacillus rhamnosus que fortalece la integridad de la barrera intestinal, son herramientas clave en la prevención y manejo de la enfermedad de Alzheimer.

Enfermedad de Parkinson
La enfermedad de Parkinson es el segundo trastorno neurodegenerativo más frecuente, con una prevalencia estimada de aproximadamente el 1 % en personas mayores de 65 años. Su carga global se ha más que duplicado en las últimas décadas y se proyecta que continúe en aumento en las generaciones futuras, impulsada principalmente por el envejecimiento progresivo de la población mundial. Se trata de una enfermedad multifactorial, en la que interactúan factores genéticos y ambientales.
La alteración estructural desempeña un papel clave
La α-sinucleína es una proteína presente en las neuronas del sistema nervioso central y del sistema nervioso entérico, cuya alteración estructural desempeña un papel clave en la enfermedad de Parkinson. En esta patología, la α-sinucleína puede sufrir un proceso de mal plegamiento que favorece su acumulación en forma de cuerpos de Lewy, especialmente en las neuronas dopaminérgicas de la sustancia negra, aunque también en otros circuitos neuronales.
La α-sinucleína alterada puede desplazarse hacia el cerebro a través del nervio vago, que conecta directamente el intestino con el tronco encefálico. Desde allí, la proteína patológica se disemina progresivamente a otras regiones del sistema nervioso central, conduciendo la evolución de la enfermedad. La proteína mal plegada induce cambios estructurales en proteínas normales, amplificando el daño neuronal. Como consecuencia de estos procesos, se desarrollan los síntomas motores característicos del Parkinson, como bradicinesia, temblores, rigidez y alteraciones de la marcha, junto con manifestaciones no motoras que incluyen trastornos gastrointestinales, disfunción urinaria, alteraciones del olfato y deterioro cognitivo. El compromiso simultáneo de los sistemas nervioso central, periférico y entérico refuerza la importancia del eje intestino–cerebro en la comprensión integral de la enfermedad de Parkinson.
El mal plegamiento del péptido β-amiloide se asocia al deterioro cognitivo y demencia
El plegamiento anómalo de la α-sinucleína puede iniciarse a nivel intestinal. En esta patología se ha demostrado una disbiosis de la microbiota, caracterizada por un aumento de bacterias coliformes y otras bacterias Gram negativas, lo que se asocia a una mayor liberación de LPS, componentes de la pared bacteriana. El incremento de la permeabilidad intestinal facilita el pasaje de estos LPS desde la luz intestinal hacia la circulación sistémica, promoviendo un estado de inflamación crónica y estrés oxidativo que contribuye tanto a la inflamación periférica como a la neuroinflamación. En conjunto, la disbiosis intestinal, el aumento de LPS y la inflamación persistente generan un entorno que favorece el plegamiento anómalo de la α-sinucleína en las neuronas del sistema nervioso entérico, desde donde la proteína patológica puede propagarse hacia el sistema nervioso central. A su vez, la inflamación crónica sistémica favorece la disrupción de la BHE y la activación microglial —proceso mediante el cual las células inmunes del sistema nervioso central adoptan un estado reactivo y liberan mediadores proinflamatorios—, generando un entorno neuroinflamatorio que altera la homeostasis neuronal y promueve el mal plegamiento del péptido β-amiloide el cual se asocia al deterioro cognitivo y demencia que también puede presentarse en esta patología.
Rol clave en la regulación de los circuitos neuronales
Se ha reportado una disminución de Prevotella spp, bacteria asociada al metabolismo de polisacáridos y vitaminas, así como una disminución de la producción de AGCC y de metabolitos neuroactivos, entre ellos el ácido γ-aminobutírico (GABA). Este neurotransmisor inhibitorio cumple un rol clave en la regulación de los circuitos neuronales, cuya alteración se ha vinculado con la disfunción neuronal observada en la enfermedad de Parkinson. La reducción de Prevotella spp. también se asocia con una menor síntesis de mucina, glucoproteínas que recubren el epitelio intestinal y contribuyen al mantenimiento de la integridad de la barrera intestinal.
Relación entre la disbiosis de la microbiota intestinal y los procesos neurodegenerativos
La asociación entre las enfermedades inflamatorias intestinales y la enfermedad de Parkinson se encuentra respaldada por evidencia epidemiológica que demuestra una mayor incidencia de esta patología en pacientes con enfermedad de Crohn y colitis ulcerosa. La mayor permeabilidad de la barrera intestinal y la inflamación sistémica características de estos trastornos refuerzan la relación entre la disbiosis de la microbiota intestinal y los procesos neurodegenerativos. En concordancia, un estudio danés de 40 años de seguimiento reveló que las personas con enfermedades inflamatorias intestinales presentan un 22 % más de riesgo de desarrollar enfermedad de Parkinson en comparación con individuos sin estas afecciones.
Las intervenciones con prebióticos y probióticos se proponen como una estrategia terapéutica complementaria orientada a revertir la disbiosis de la microbiota intestinal, favoreciendo el crecimiento de bacterias beneficiosas y la producción de AGCC. De esta forma se mejora la integridad de la barrera epitelial intestinal, limita la traslocación de LPS, atenúa la inflamación sistémica y modula los procesos inflamatorios y neurodegenerativos implicados en la progresión de la enfermedad de Parkinson.
Característica
Enfermedad de Alzheimer
Enfermedad de Parkinson
Tipo de enfermedad
Neurodegenerativa progresiva.
Neurodegenerativa progresiva.
Péptido/ Proteína implicada
Péptido beta-amiloide (Aβ) (mal plegamiento, agregación en oligómeros, fibrillas formando placas amieloides; acumulación por falla de la eliminación).
Proteína α-sinucleína (mal plegamiento, agregación en oligómeros, fibrillas formando los cuerpos de Lewy; acumulación por falla de la eliminación).
Síntomas principales
Deterioro de memoria, cognición, capacidades funcionales y conducta.
Bradicinesia, temblores, rigidez, alteraciones de la marcha y síntomas no motores como trastornos gastrointestinales
Microbiota intestinal
Disbiosis asociada al aumento de LPS y TMAO, disminución de bacterias productoras de butirato (AGCC).
Mayor permeabilidad intestinal y de la BHE – Neuroinflamación.
Disbiosis asociada al aumento de LPS, disminución de GABA y de Prevotella spp, menor producción de AGCC.
Mayor permeabilidad intestinal y de la BHE – Neuroinflamación.
Estrategia terapéutica
Prebióticos y Probióticos.
Prebióticos y Probióticos.
Prebióticos y Probióticos en la prevención y control de enfermedades neurodegenerativas
La integridad de la barrera intestinal es crucial para el funcionamiento del eje intestino-cerebro. Factores como la disbiosis, el estrés crónico, la edad avanzada y una baja ingesta de fibra deterioran esta barrera, aumentando su permeabilidad y favoreciendo la entrada de endotoxinas proinflamatorias como los LPS. Las dietas ricas en fibra, particularmente aquellas que incluyen prebióticos bifidogénicos como la inulina, aumentan notablemente la abundancia de bacterias productoras de AGCC. Esto no solo reduce la permeabilidad intestinal, sino que también disminuye biomarcadores inflamatorios sistémicos asociados con la neurodegeneración.
Efectos neuroprotectores
Una microbiota intestinal equilibrada con una alta producción de AGCC ejercen efectos neuroprotectores a través de varios mecanismos, entre ellos la regulación de respuestas inflamatorias, la modulación de la respuesta inmune y de la microglía. Además, una microbiota funcionalmente saludable limita los efectos adversos de metabolitos microbianos como los LPS, regula la producción de neurotransmisores clave como serotonina y dopamina, y mantiene la integridad de la barrera intestinal y BHE. Particularmente, niveles adecuados de AGCC asociados con una mayor abundancia de bacterias beneficiosas, se vinculan con la preservación de la barrera intestinal, la reducción de la neuroinflamación y una menor susceptibilidad neuronal al daño, factores clave en enfermedades como el Alzheimer y Parkinson. La disminución de la permeabilidad intestinal como consecuencia del consumo de prebióticos y probióticos disminuye la traslocación de LPS al cerebro y la activación de procesos neuroinflamatorios, comunes en ambas patologías.
Lactobacillus rhamnosus GG
En particular, Lactobacillus rhamnosus GG ha demostrado efectos beneficiosos en la salud intestinal y cerebral. Este probiótico protege las células epiteliales intestinales, reduce marcadores inflamatorios y mejora la integridad de la barrera intestinal. A través de estos mecanismos, Lactobacillus rhamnosus GG influye positivamente en la función cognitiva. Un estudio realizado con 145 personas mostró que aquellas personas con deterioro cognitivo que recibieron Lactobacillus rhamnosus GG experimentaron una mejora significativamente mayor en la puntuación cognitiva total en comparación con el grupo placebo. Estos resultados asocian la suplementación de este probiótico con mejoras cognitivas en adultos de mediana edad y mayores con evidencia objetiva de deterioro cognitivo.
Regula activamente la síntesis y disponibilidad de neurotransmisores
Por otro lado, la microbiota intestinal regula activamente la síntesis y disponibilidad de neurotransmisores cruciales para la cognición y el estado de ánimo, como la serotonina y la dopamina, y modula la producción de GABA, esencial para el equilibrio neuronal. Géneros bacterianos como Bacteroides, Bifidobacterium y Lactobacillus influyen en la producción de estos neurotransmisores, contribuyendo al equilibrio neuroquímico necesario para la función cognitiva. Así, la disbiosis intestinal puede afectar tanto el comportamiento como la progresión del deterioro cognitivo en estas enfermedades neurodegenerativas.
En conjunto, estos mecanismos respaldan el papel de los probióticos como herramienta para modular favorablemente la microbiota intestinal, fortalecer el eje intestino-cerebro y contribuir a la prevención o atenuación de procesos asociados a la progresión de enfermedades neurodegenerativas como el Alzheimer y Parkinson.
Alimentación
La dieta ejerce un efecto rápido sobre la composición de la microbiota intestinal, promoviendo el crecimiento de determinados grupos bacterianos sobre otros y generando cambios en el pH y permeabilidad intestinal, la producción de metabolitos bacterianos y, en consecuencia, en los procesos inflamatorios. Por este motivo, la intervención nutricional se plantea como un enfoque terapéutico con impacto tanto sobre la microbiota intestinal como sobre el sistema inmunitario.

Dieta mediterránea
La dieta mediterránea muestra una evidencia científica creciente respecto de sus efectos y beneficios. Se caracteriza por un elevado aporte de carbohidratos complejos ricos en fibra, presentes en cereales, legumbres, verduras y frutas, ácidos grasos poliinsaturados con propiedades antiaterogénicas y antiinflamatorias, provenientes principalmente del aceite de oliva y los frutos secos y compuestos bioactivos con acción antioxidante, como flavonoides, fitoesteroles, terpenos y polifenoles. Asimismo, el adecuado equilibrio de micronutrientes, incluyendo vitaminas y minerales, contribuye a prevenir estados de desnutrición e inmunodeficiencia.

Patrones dietéticos occidentales
En contraste, los patrones dietéticos occidentales promueven un estado de disbiosis, caracterizado por un aumento de la proporción Firmicutes:Bacteroidetes. Este desequilibrio puede ser atenuado mediante la dieta mediterránea, que incrementa la abundancia de bacterias favorables y sus metabolitos, al tiempo que reduce la disbiosis y los niveles de LPS. Este efecto resulta relevante para el manejo dietético de diversas patologías incluyendo las neurodegenerativas, posicionando a la dieta mediterránea como una estrategia eficaz para modular la microbiota del huésped, inducir respuestas locales y sistémicas beneficiosas y mejorar la diversidad microbiana y la función de la barrera intestinal en comparación con los patrones occidentales.
Hacer click sobre el cuadro para ampliar la imagen.
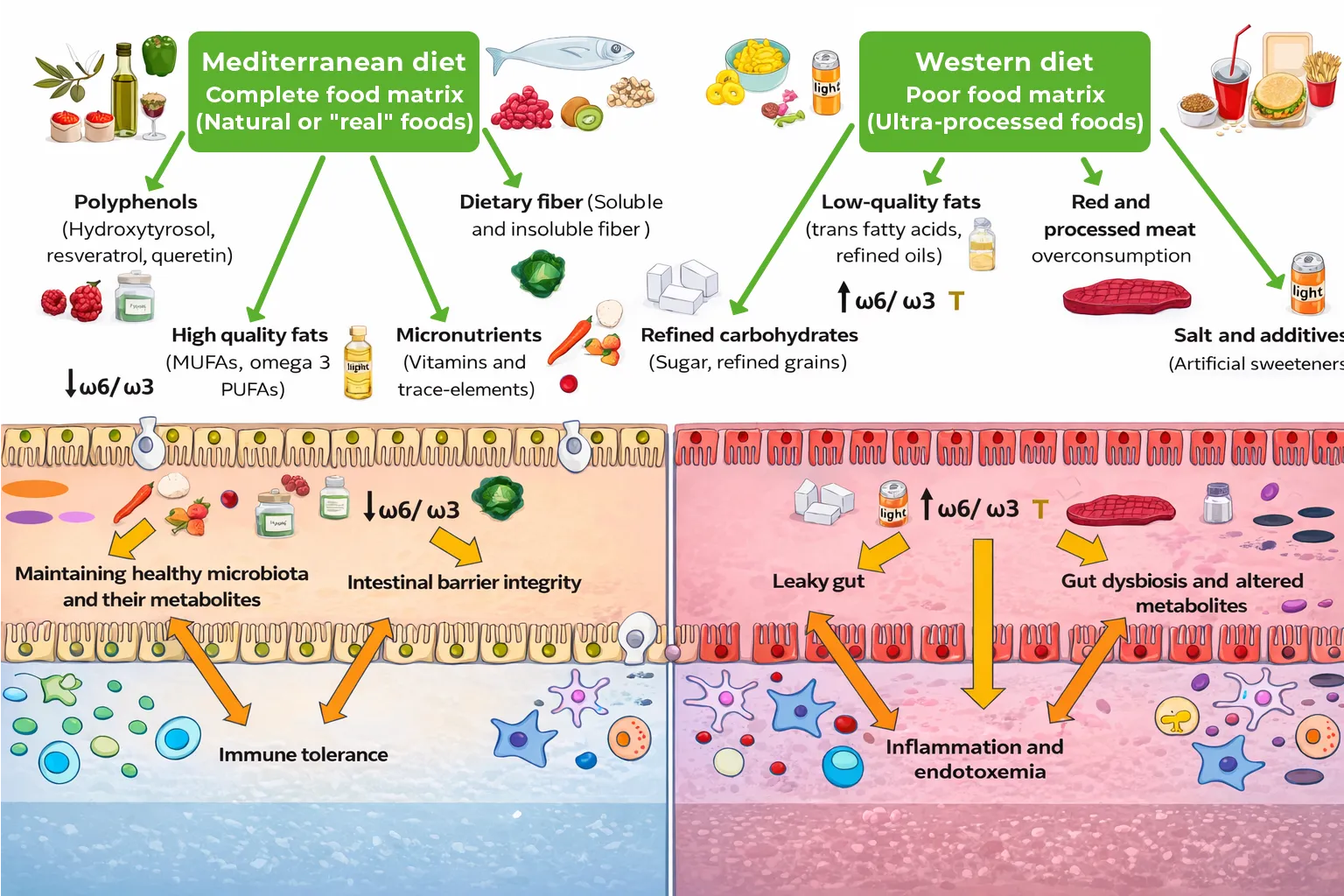
Figura 3. Principales componentes nutricionales que modulan tanto la microbiota intestinal como el sistema inmunitario. La dieta mediterránea, rica en alimentos de origen vegetal, presenta polifenoles, grasas de alta calidad (con alto contenido omega 3), micronutrientes como vitaminas y oligoelementos, y fibra dietética que, en una matriz alimentaria adecuada y completa, determinarán sus propiedades beneficiosas para mantener la microbiota intestinal, la eubiosis y sus productos metabólicos, junto con la integridad de la barrera intestinal y la respuesta inmunitaria. Por otro lado, las dietas occidentales y los alimentos ultraprocesados, caracterizados por bajos niveles de fibra dietética y micronutrientes, presentan una gran variedad de componentes nutricionales, incluyendo carbohidratos refinados (azúcar y cereales refinados), grasas de baja calidad (ácidos grasos trans y una proporción excesiva de omega 6/omega 3 debido a los aceites refinados), sal y aditivos poco saludables y, finalmente, un consumo excesivo de carne roja y procesada. Además, presentan una matriz alimentaria pobre que tendrá efectos perjudiciales en la barrera intestinal, provocando un intestino permeable, disbiosis intestinal y metabolitos alterados, lo que además provoca una inflamación local y la presencia de LPS en el torrente sanguíneo que contribuye a la endotoxemia sistémica y la inflamación crónica.
García-Montero C, Fraile-Martínez O, Gómez-Lahoz AM, Pekarek L, Castellanos AJ, Noguerales-Fraguas F, Coca S, Guijarro LG, García-Honduvilla N, Asúnsolo A, et al. Nutritional Components in Western Diet Versus Mediterranean Diet at the Gut Microbiota–Immune System Interplay. Implications for Health and Disease. Nutrients. 2021; 13(2):699. https://doi.org/10.3390/nu13020699
Conclusión
Las enfermedades neurodegenerativas, como la enfermedad de Alzheimer y la enfermedad de Parkinson, se caracterizan por procesos progresivos de neuroinflamación, deterioro cognitivo y disfunción neuronal. En este contexto, la evidencia científica reciente señala que la microbiota intestinal desempeña un papel central en su fisiopatología a través del eje microbiota–intestino–cerebro, un sistema de comunicación bidireccional que integra señales inmunitarias, metabólicas, neuroendócrinas y neuronales.
Las alteraciones en la composición y funcionalidad de la microbiota intestinal, asociadas al envejecimiento, a factores ambientales y a patrones dietéticos inadecuados, favorecen la disbiosis intestinal, la pérdida de integridad de la barrera intestinal y de la barrera hematoencefálica, y la activación sostenida de procesos inflamatorios. Estas alteraciones promueven un estado de inflamación crónica de bajo grado, la translocación de endotoxinas bacterianas como el lipopolisacárido hacia la circulación sistémica que contribuyen de manera significativa a la progresión de la neurodegeneración.
Los ácidos grasos de cadena corta, especialmente el butirato, generado a partir de la fermentación de fibras prebióticas como la INULUNA, contribuyen al mantenimiento de la integridad de las barreras biológicas, a la regulación de la respuesta inmunitaria y a la atenuación de la neuroinflamación. La reducción de bacterias productoras de AGCC observada tanto en la enfermedad de Alzheimer como en la enfermedad de Parkinson refuerza la importancia de preservar una microbiota funcionalmente equilibrada para sostener la homeostasis cerebral. Las dietas ricas en fibra, particularmente aquellas que incluyen prebióticos bifidogénicos como la INULINA, aumentan notablemente la abundancia de bacterias productoras de AGCC. Dentro de los probióticos, se destaca la cepa Lactobacillus rhamnosus GG la cual ha mostrado efectos positivos sobre la integridad intestinal, la inflamación y la función cognitiva, respaldando su potencial aplicación en contextos de deterioro cognitivo.
La alimentación es un factor modulador central del eje microbiota–intestino–cerebro. Patrones dietéticos como la dieta mediterránea caracterizada por un predominio de alimentos de origen vegetal, ricos en fibra, grasas saludables y compuestos bioactivos, favorecen la eubiosis intestinal, la producción de metabolitos beneficiosos y la reducción de procesos inflamatorios asociados a la neurodegeneración. En conjunto, las estrategias nutricionales, junto con la incorporación de prebióticos y probióticos, representan herramientas relevantes en la prevención y la atenuación de la progresión de las enfermedades neurodegenerativas.
Fuentes
Wang M, Zeng Y, Jin Y, Wu J, Li J. Progreso y perspectivas sobre el eje estrógeno-microbiota-cerebro en la enfermedad de Alzheimer. Neuroquímica Res. 2025 26 de noviembre; 51(1):3. doi: 10.1007/s11064-025-04613-6. PMID: 41296090.
Loh, J.S., Mak, W.Q., Tan, L.K.S. y otros. Eje microbiota–intestino–cerebro y sus aplicaciones terapéuticas en enfermedades neurodegenerativas. Objetivo de transducción de siglas Ther 9, 37 (2024). https://doi.org/10.1038/s41392-024-01743-1
Heravi FS, Naseri K, Hu H. Gut Microbiota Composition in Patients with Neurodegenerative Disorders (Parkinson’s and Alzheimer’s) and Healthy Controls: A Systematic Review. Nutrients. 2023 Oct 13;15(20):4365. doi: 10.3390/nu15204365. PMID: 37892440; PMCID: PMC10609969
National Institute of Environmental Health Sciences. (2023). Neurodegenerative diseases. National Institutes of Health. https://www.niehs.nih.gov/research/supported/health/neurodegenerative
Klann EM, Dissanayake U, Gurrala A, Farrer M, Wagle Shukla A, Ramirez-Zamora A, Mai V, Vedam-Mai V. The Gut-Brain Axis and Its Relation to Parkinson’s Disease: A Review. Front Aging Neurosci. 2022 Jan 7;13:782082. doi: 10.3389/fnagi.2021.782082. PMID: 35069178; PMCID: PMC8776990.
García-Montero C, Fraile-Martínez O, Gómez-Lahoz AM, Pekarek L, Castellanos AJ, Noguerales-Fraguas F, Coca S, Guijarro LG, García-Honduvilla N, Asúnsolo A, et al. Nutritional Components in Western Diet Versus Mediterranean Diet at the Gut Microbiota–Immune System Interplay. Implications for Health and Disease. Nutrients. 2021; 13(2):699. https://doi.org/10.3390/nu13020699
Sanborn V, Azcarate-Peril MA, Updegraff J, Manderino L, Gunstad J. Randomized Clinical Trial Examining the Impact of Lactobacillus rhamnosus GG Probiotic Supplementation on Cognitive Functioning in Middle-aged and Older Adults. Neuropsychiatr Dis Treat. 2020 Nov 13;16:2765-2777. doi: 10.2147/NDT.S270035. PMID: 33223831; PMCID: PMC7671471.
Spielman, L.J., Gibson, D.L., Klegeris, A., Unhealthy gut, unhealthy brain: The role of the intestinal microbiota in neurodegenerative diseases, Neurochemistry International (2018), doi: 10.1016/j.neuint.2018.08.005