La microbiota intestinal en la longevidad: Relación de la microbiota y las enfermedades asociadas al envejecimiento
La OMS describe el envejecimiento como el resultado de la acumulación progresiva de daños moleculares y celulares a lo largo del tiempo, lo que provoca un descenso gradual de las capacidades físicas y mentales aumentando el riesgo de desarrollar enfermedades.
En las últimas décadas, el mundo ha experimentado un cambio demográfico sostenido: la proporción de personas mayores aumenta de forma continua y se proyecta que, para el 2030, 1 de cada 6 personas tendrá 60 años o más. Hacia 2050, este grupo prácticamente se duplicará. Aunque este proceso comenzó en países de ingresos altos, el crecimiento más acelerado se observa actualmente en países de ingresos bajos y medianos, que concentrarán la mayor parte de la población mayor en las próximas décadas. Este escenario describe un envejecimiento poblacional global con implicancias significativas para los sistemas de salud y las estructuras sociales.
Factores genéticos, ambientales y el estilo de vida (dieta, actividad física, nivel de estrés) condicionan la manera en que se desarrolla el envejecimiento. La interacción entre estos elementos determina diferencias significativas entre individuos, lo que explica por qué algunas personas experimentan un envejecimiento más saludable que otras. Entre los múltiples factores que modulan este proceso, la microbiota intestinal ha cobrado especial relevancia en los últimos años.
Su composición, diversidad y funcionalidad se modifican con la edad, y estas alteraciones impactan directamente sobre la inflamación sistémica, la inmunidad y la susceptibilidad a enfermedades crónicas y degenerativas.
Modificaciones en el metabolismo y la función intestinal
Con el paso del tiempo, la microbiota intestinal sufre una transformación progresiva que refleja modificaciones en el metabolismo y la función intestinal. Diversos estudios han mostrado que las personas mayores presentan una menor diversidad microbiana, un aumento de especies proinflamatorias asociado a la disfunción inmunitaria denominada “inflammaging”, caracterizada por una inflamación crónica de bajo grado y la disminución de las respuestas inmunitarias adaptativas, así como una reducción de microorganismos productores de los ácidos grasos de cadena corta (AGCC), metabolitos clave para mantener la integridad del epitelio intestinal y controlar la inflamación local. Esto conlleva a importantes alteraciones como:
Inflamación crónica de bajo grado
Muchas enfermedades características relacionadas con la edad están relacionadas con niveles crónicos de inflamación de bajo grado como las enfermedades cardiovasculares, síndrome metabólico y enfermedad renal crónica. La inflamación asociada con el envejecimiento también afecta el proceso fisiológico, como la síntesis de proteínas musculares que puede conducir a la sarcopenia y contribuir a la fragilidad.
Aumento de la permeabilidad intestinal
Permite el paso de bacterias y de sus componentes hacia la circulación sistémica. Entre estos, los lipopolisacáridos (LPS) actúan como un potente patrón molecular asociado a patógenos que se une a los receptores de reconocimiento de patrones en células inmunes y adipocitos. Esta interacción activa la producción de citoquinas proinflamatorias y desencadena una inflamación sistémica persistente de bajo grado, típica del envejecimiento y vinculada a patologías como el síndrome metabólico, la resistencia a la insulina y las enfermedades cardiovasculares. Se ha demostrado que los niveles sanguíneos de LPS se correlacionan con la extensión de la amiloidosis cerebral observada en pacientes con enfermedad de Alzheimer. En estos pacientes se han encontrado concentraciones séricas más bajas de ácidos biliares primarios y mayores niveles de ácidos biliares secundarios, los cuales se originan en el microbioma intestinal y se translocan al cerebro. Los aumentos en ácidos biliares secundarios específicos, como el ácido desoxicólico, están fuertemente asociados con el deterioro cognitivo.
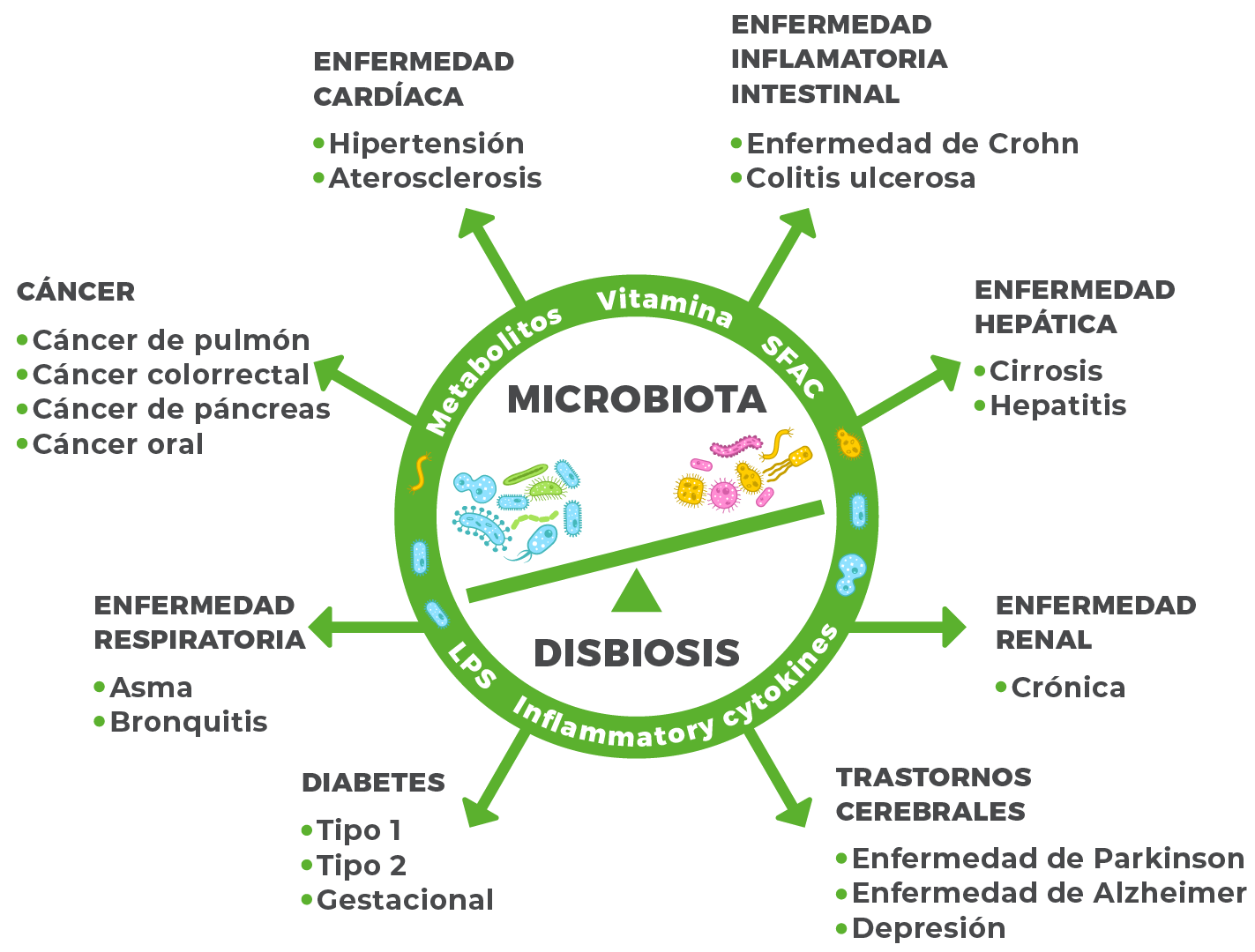
Hacer click sobre el cuadro para ampliar la imagen.
Figura 1. La disbiosis de la microbiota contribuye a diversas enfermedades.
(Hou K, Wu ZX, Chen XY, Wang JQ, Zhang D, Xiao C, Zhu D, Koya JB, Wei L, Li J, Chen ZS. Microbiota in health and diseases. Signal Transduct Target Ther. 2022 Apr 23;7(1):135. doi: 10.1038/s41392-022-00974-4. PMID: 35461318; PMCID: PMC9034083)
Un poco de historia: Evolución de la microbiota intestinal humana
La microbiota asociada ancestralmente al Homo sapiens ha ido cambiando a lo largo del tiempo, así como su transmisión vertical de padres a hijos.
Los avances médicos y farmacológicos (antibióticos), y las medidas de salud pública para proveer suministro de agua potable, prevenir la contaminación de alimentos, etc., han logrado el control de las grandes plagas infecciosas que asolaban a nuestros antepasados hace apenas unas décadas.
Factores importantes como la menor exposición a microbios del ambiente y el uso frecuente de antibióticos alteraron la transmisión natural de microorganismos entre personas y generaciones. Como consecuencia, la microbiota del ser humano moderno es menos diversa y más inestable, este desequilibrio se asocia con la creciente aparición de las nuevas “plagas” del mundo actual: las enfermedades crónicas no transmisibles, como alergias, enfermedades autoinmunes, obesidad, enfermedad inflamatoria intestinal y otros trastornos vinculados con la inflamación de bajo grado.
Modificación del microbioma a lo largo de la vida del individuo
El desarrollo del microbioma intestinal puede comenzar antes del nacimiento, ya que el feto está expuesto a metabolitos microbianos maternos e incluso a comunidades bacterianas en el útero. Al nacer, se produce una importante transferencia de microbiota de la madre al bebé, la cual se ve influenciada por el tipo de parto (vaginal o cesárea) y posteriormente por la forma de alimentación (lactancia materna o fórmula). La siguiente transición relevante en el microbioma ocurre con la introducción de alimentos sólidos y el destete, momento en que la composición microbiana pasa a estar determinada por la dieta y el entorno al que el niño está expuesto.
La configuración del microbioma en estas etapas iniciales resulta de particular interés debido a la producción de metabolitos beneficiosos derivados de la fermentación de carbohidratos no digeribles, especialmente los AGCC. Estos compuestos ejercen efectos protectores a largo plazo, contribuyendo al mantenimiento de la homeostasis intestinal y a la prevención de enfermedades metabólicas e inmunológicas en etapas posteriores de la vida.
Composición de la microbiota y producción de AGCC en diferentes etapas de la vida
Patrones favorables
Edad
Primera etapa de la vida (0 – 3 años)
Adulto
Adulto mayor
AGCC
Producción de acetato debido al consumo de oligosacáridos de la leche humana por Bifidobacterias.
Aumento de Firmicutes y Bacteroidetes, incremento de propionato y butirato que se mantiene estable con el tiempo.
Disminución de la producción de propionato y butirato.
Microbiota intestinal
Cambios significativos en la abundancia de Proteobacterias y Actinobacterias en un corto periodo de tiempo durante la lactancia materna. Esto se modifica con la introducción a alimentos sólidos.
Recién nacido
Lactancia materna
Alimentos sólidos
Introducción a una dieta más variada que provoca cambios en la microbiota intestinal.
Adulto

Disminución de la diversidad microbiana y aumento de Proteobacterias.
Adulto mayor
Actinobacteria
Bacteroidetes
Firmicutes
Proteobacteria
Otros
Influencia determinante sobre la producción
de AGCC
La microbiota intestinal constituye la principal fuente de bacterias productoras de AGCC, generados a través de la degradación de diversos sustratos, principalmente polisacáridos no digeribles, como las fibras prebióticas. La concentración de estos metabolitos fluctúa a lo largo de la vida y guarda una estrecha relación con los cambios en la composición del microbioma intestinal, que también se modifica con el avance del ciclo vital. En este contexto, la diversidad y calidad de la dieta ejercen una influencia determinante sobre la producción de AGCC, en función de la cantidad y tipo de sustratos disponibles para las bacterias.
Tres principales AGCC y las variaciones en la microbiota asociadas a la edad
Los niveles intestinales de acetato, propionato y butirato —los tres principales AGCC— se ven modulados por las variaciones en la microbiota asociadas a la edad. El acetato predomina en las primeras etapas de la vida, siendo el principal producto de las cepas de Bifidobacteria característica de la microbiota infantil. La producción de acetato depende, además, de sustratos específicos conocidos como fibras bifidogénicas, entre las que destacan la inulina y los galacto-oligosacáridos.
Maduración metabólica y funcional del ecosistema intestinal
Con el cese de la lactancia materna y la incorporación de una dieta más variada, aumentan los niveles de propionato y butirato intestinal, reflejando la diversificación de la microbiota. En esta etapa se observa un incremento en la proporción de Firmicutes, lo que indica una maduración metabólica y funcional del ecosistema intestinal.
Butirato es el que ejerce
el mayor impacto
fisiológico
Entre los tres AGCC principales, el butirato es el que ejerce el mayor impacto fisiológico. Las comunidades microbianas productoras de butirato son esenciales para mantener un entorno intestinal saludable, ya que limitan la colonización y proliferación de bacterias potencialmente patógenas. La producción de butirato resulta fundamental para el metabolismo energético de los colonocitos, al favorecer el consumo de oxígeno epitelial y mantener un ambiente anaeróbico que dificulta el crecimiento de patógenos aeróbicos oportunistas, como Salmonella y E. coli.
Regulación de la respuesta inmunitaria y la homeostasis intestinal
Los AGCC desempeñan un papel esencial en la regulación de la respuesta inmunitaria y la homeostasis intestinal. Entre sus múltiples funciones destacan sus efectos antiinflamatorios y su capacidad para mantener la integridad de la barrera epitelial, prevenir la translocación bacteriana y modular la actividad de las células inmunes. Cuando la producción o el equilibrio de estos metabolitos se alteran, se desencadenan procesos inflamatorios crónicos que predisponen al desarrollo de enfermedades metabólicas, inmunológicas y degenerativas.
Microbiota intestinal de las personas mayores
Aunque la composición de la flora intestinal suele ser bastante estable en individuos sanos, puede verse alterada por numerosos factores endógenos y exógenos, tales como:
Trastornos del peristaltismo
Cáncer
Cirugías del estómago o del intestino delgado
Enfermedades hepáticas o renales
Anemia pernicios
Radioterapia
Estrés emocional
Alteraciones del sistema inmunológico
Administración de antibióticos
Envejecimiento
En las personas mayores las Bifidobacterias disminuyen, aumentando significativamente los Lactobacilos, Estreptococos y Enterobacterias. Este fenómeno se considera el resultado del envejecimiento que podría acelerar la senescencia.
Las Bifidobacterias deberían estar presentes en el intestino grueso como bacterias intestinales beneficiosas a lo largo de la vida humana, por lo cual su reducción o desaparición indicaría un estado no saludable. De hecho, se ha registrado una mayor proporción de Bifidobacterias en personas mayores de 100 años, lo cual sugiere que la longevidad de los centenarios podría estar vinculada a características distintivas dentro de su microbiota intestinal. Las bifidobacterias ayudan a mantener el equilibrio microbiano intestinal, suprimir bacterias patógenas, mejorar la digestión y fortalecer el sistema inmunitario.
El rol de la microbiota en la salud
Mantenimiento de la barrera intestinal y mecanismos inmunes de defensa
La microbiota ejerce un efecto trófico sobre el epitelio intestinal, favoreciendo la proliferación de las células epiteliales y el mantenimiento de las uniones estrechas. La mucosa intestinal está cubierta por un gel rico en mucinas (MUC2) que actúa como un escudo frente a: bacterias y virus, ácidos biliares, enzimas digestivas y sustancias irritantes de la dieta. La capa de moco mantiene a las bacterias separadas del epitelio, impide la adhesión de patógenos, reduce la translocación de endotoxinas bacterianas (LPS) y disminuye la activación inflamatoria innecesaria. El butirato es el regulador más potente de la secreción de moco, contribuyendo así al fortalecimiento de la barrera epitelial frente a agentes exógenos. Sin la capa mucosa el epitelio sería vulnerable a lesiones y erosiones.
La producción de inmunoglobulina A secretora (IgAs) constituye otro mecanismo defensivo que limita el acceso de bacterias a la mucosa. Éstas son transportadas a través del epitelio uniéndose a bacterias intestinales colaborando con el control de patógenos, neutralizando toxinas y favoreciendo su eliminación. Los macrófagos fagocitan y eliminan los microorganismos que hubieran entrado a través del epitelio intestinal.
La homeostasis intestinal se mantiene mediante un sistema de controles y equilibrios entre las células T efectoras inflamatorias, que incluyen las células Th1 (CD4+ y CD8+ que migran al epitelio convirtiéndose en linfocitos intraepiteliales), las células Th17 y las células T reguladoras Foxp3+ antiinflamatorias (Tregs). Además, las células dendríticas activadas interactúan con células B y T de las placas de Peyer, induciendo la producción de inmunoblogulinas, tanto las secretoras como las que ejercen una protección sistémica.
Las células linfoides innatas (CLI) que se localizan en el epitelio intestinal están involucradas en el mantenimiento de respuestas inmunes apropiadas a los distintos microorganismos, potenciando la inmunidad adaptativa, y regulando la inflamación y la reparación de tejidos en la mucosa intestinal. Las funciones de las CLI también están reguladas por la microbiota.
Las interacciones entre la microbiota y las células del sistema inmune innato se producen a través de receptores de reconocimiento de patrones moleculares microbianos (TLR, NODs, inflamasomas, etc.) o de metabolitos (triptófano, indoles, butirato) producidos por la microbiota. Estos estímulos activan tanto las funciones de barrera anteriormente descritas, como la síntesis de otros mediadores (citoquinas, moléculas co-estimuladoras, etc.) que regulan la respuesta de células inmunes especializadas del tejido linfoide asociado al intestino, coordinando sus acciones para evitar la invasión de patógenos y favorecer el desarrollo de tolerancia a antígenos inocuos.
Regulación endócrino – metabólica
La microbiota a través de la generación de AGCC, ejerce efectos tróficos sobre la mucosa intestinal y activa diversos receptores (GPR41 y GPR43), que estimulan la producción de hormonas enteroendócrinas por parte de las células L, como el péptido similar al glucagón (GLP-1) o el péptido tirosina-tirosina (PYY). Los AGCC y los péptidos enteroendócrinos contribuyen a regular la homeostasis energética, modulando aspectos como el metabolismo de la glucosa, la sensibilidad a la insulina, la termogénesis y el apetito, a través de efectos endócrinos sobre órganos periféricos (hígado y el tejido adiposo blanco y marrón), y mediante vías señalización neural (sistema nervioso entérico y autónomo) que llegan al sistema nervioso central, donde se integran las señales que regulan el balance energético a corto (GLP-1) y largo plazo (insulina, leptina). Además, la microbiota intestinal participa en el metabolismo y en la circulación entero-hepática de las sales biliares, y contribuye a la generación de ácidos biliares secundarios, que interaccionan con el receptor TGR5, induciendo diferenciación y aumento de células L y secreción de GLP-1, lo que también influye beneficiosamente en la tolerancia oral a la glucosa.
Las células epiteliales también están implicadas en la síntesis de glucocorticoides, que desempeñan una función anti-inflamatoria y endócrina, y tanto su síntesis como la expresión de sus receptores puede verse modificada por la composición de la microbiota intestinal.
Síntesis de neurotransmisores
La microbiota también interviene de forma directa o indirecta en la síntesis de compuestos neuroactivos, incluidos distintos neurotransmisores (serotonina, dopamina, ácido γ-aminobutírico [GABA], etc.) que influyen en las funciones cerebrales, el comportamiento, el metabolismo y la inmunidad. La influencia de la microbiota en la síntesis de serotonina parece particularmente relevante ya que hasta un 90% de este neurotransmisor, que ejerce funciones claves a nivel central y periférico, se sintetiza en el intestino. A nivel del sistema nervioso central, la serotonina es clave en la regulación del estado de ánimo, el apetito y las funciones cognitivas y a nivel intestinal regula la inflamación y la motilidad. La microbiota intestinal puede estar implicada tanto en la reducción de los niveles de serotonina (por su capacidad de metabolizar el triptófano que actúa como precursor), como en su producción estimulando la expresión de los genes (triptófano 1 hidroxilasa) implicados en su síntesis, a través del efecto estimulador de los AGCC. La modulación microbiana de la biosíntesis de serotonina y de la expresión de sus receptores mitiga la inflamación intestinal y los síntomas depresivos.
Diversas bacterias intestinales codifican tirosinasas capaces de transformar la tirosina en L-dihidroxifenilalanina (L-DOPA), que a su vez conduciría a la síntesis de catecolaminas, como dopamina, norepinefrina y epinefrina. La dopamina tiene una importante función en el sistema de recompensa, implicado en la regulación del comportamiento alimentario y también en el estado de ánimo.
El GABA es producido por diversas bacterias intestinales a través de la descarboxilación del glutamato por acción de la enzima glutamato descarboxilasa, implicada en la tolerancia al pH ácido y el mantenimiento de la homeostasis intracelular bacteriana. El GABA es un importante neurotransmisor con efectos inhibidores en el cerebro, y su disfunción está implicada en enfermedades como el autismo y la esquizofrenia.
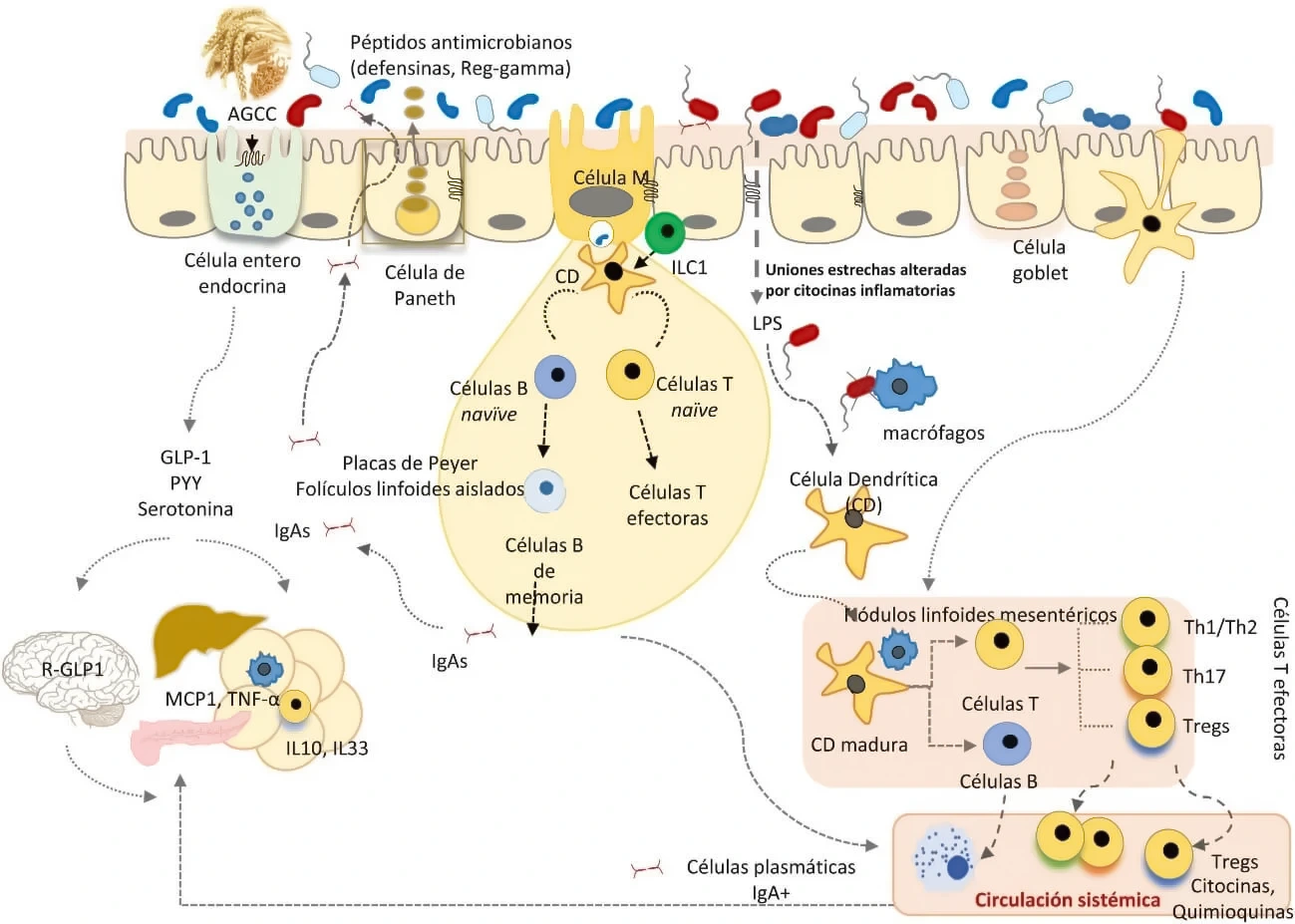
Hacer click sobre el cuadro para ampliar la imagen.
Figura 2. Representación esquemática del efecto de la microbiota y sus metabolitos sobre la función de la barrera intestinal y los sistemas inmunológico y neuroendócrinos.
(Álvarez, J., Fernández Real, J. M., Guarner, F., Gueimonde, M., Rodríguez, J. M., Saenz de Pipaón, M., et al. (2021). Microbiota intestinal y salud. Gastroenterología y Hepatología, 44(7), 519-535. doi:10.1016/j.gastrohep.2021.06.002)
Restauración de la microbiota y su papel en la promoción de la salud
Intervenciones prebióticas y probióticas para mejorar la microbiota en el envejecimiento

La dieta puede influir y modular la microbiota intestinal de los individuos, y en los adultos mayores, esto es especialmente relevante debido a la reducción natural de la abundancia y diversidad microbiana asociada al envejecimiento. En este contexto, la fibra prebiótica, los suplementos de fibra prebiótica como la INULINA y los probióticos desempeñan un rol clave en la restauración del equilibrio microbiano. Los prebióticos y los probióticos contribuyen a revertir este patrón al favorecer el crecimiento de bacterias beneficiosas y aumentar la diversidad global, lo cual se refleja en el incremento del índice de Shannon —medida utilizada para cuantificar la biodiversidad considerando la riqueza de especies y su abundancia relativa— en individuos suplementados.
La inulina, en particular, actúa como una fibra bifidogénica, ya que es utilizada selectivamente por las Bifidobacterias, favoreciendo su crecimiento y actividad metabólica. Estas bacterias deberían mantenerse presentes en el intestino grueso a lo largo de la vida, por lo que su disminución o desaparición indica un estado no saludable. Su abundancia desciende de manera gradual con el envejecimiento, mientras que una alta presencia de Bifidobacterias se considera un sello distintivo de longevidad y longevidad extrema. El aumento de estas bacterias potencia la fermentación de fibras y la producción de AGCC, compuestos que suelen estar disminuidos en los adultos mayores lo cual se asocia con un deterioro metabólico, mayor permeabilidad intestinal e inflamación crónica de bajo grado.


Suplementación con prebióticos y probióticos
Incrementa la síntesis de AGCC, metabolitos que mantienen la integridad de la barrera epitelial.
Reducen la permeabilidad intestinal y previenen la translocación bacteriana.
Regulan la actividad de las células inmunes y fortalecen el ambiente anaeróbico del colon, dificultando el crecimiento de patógenos oportunistas como Salmonella y Escherichia coli.
Mejoran el metabolismo de la glucosa y los lípidos y reducen la inflamación crónica de bajo grado, contribuyendo a prevenir enfermedades metabólicas, inmunológicas y degenerativas relacionadas con la edad.
En conjunto, las intervenciones dietarias mediante la suplementación con prebióticos y probióticos constituyen una herramienta eficaz para promover la salud intestinal y sistémica en adultos mayores.
La recuperación del equilibrio del microbioma favorece la salud de los adultos mayores, contribuyendo a un envejecimiento más saludable gracias a las funciones del microbioma y los metabolitos que promueven el correcto funcionamiento del organismo.
Conclusión
La microbiota intestinal ha coevolucionado junto al ser humano adaptándose a los cambios en la dieta, el entorno y los estilos de vida. En las sociedades ancestrales caracterizadas por una alimentación rica en fibras y una estrecha relación con la naturaleza, había una mayor diversidad microbiana, que se fue perdiendo con el tiempo debido a hábitos modernos, cambios en la dieta como la disminución del consumo de fibras, uso de antibióticos, etc. Esta pérdida de diversidad microbiana se relaciona con alteraciones inmunes, metabólicas y neuroendócrinas que impactan directamente en la salud y la longevidad.
A lo largo de la vida, la composición de la microbiota también se va modificando. Una menor diversidad microbiana con disminución de Bifidobacterias junto con un aumento de especies proinflamatorias, se correlaciona con disfunciones inmunitarias y una menor producción AGCC. El aumento en la permeabilidad intestinal es el mejor marcador fisiopatológico del envejecimiento, reflejando la pérdida de integridad de la barrera intestinal.
Los AGCC, metabolitos derivados de la fermentación de fibras prebióticas como la inulina, ejercen efectos tróficos sobre la mucosa intestinal, promoviendo la producción de moco, integridad epitelial y reforzando las uniones estrechas, lo que disminuye la translocación bacteriana y de LPS. Además, los AGCC reducen el pH intestinal, creando un ambiente menos favorable para los microorganismos patógenos. También estimulan la motilidad intestinal y ejercen acción antiinflamatoria al regular la expresión de citoquinas proinflamatorias. Sus efectos antiinflamatorios permiten modular la inflamación crónica de bajo grado propia del envejecimiento. A nivel neuroendócrino, la microbiota y los AGCC modulan la síntesis de neurotransmisores como la serotonina y el GABA, fortaleciendo el eje intestino-cerebro y contribuyendo al equilibrio cognitivo y emocional en la edad avanzada.
La modulación del microbioma intestinal mediante la ingesta de prebióticos y probióticos es una herramienta eficaz para preservar las funciones metabólicas, inmunológicas y neuroendócrinas. La inulina es una fibra prebiótica bifidogénica que ayuda a aumentar las Bifidobacterias favoreciendo el aumento de la diversidad y la abundancia de la microbiota intestinal. La administración de probióticos contrarresta procesos propios de la inmunosenescencia mediante la regulación de citoquinas, la mejora de la integridad epitelial intestinal y la modulación del sistema inmune. Estas acciones disminuyen la inflamación sistémica persistente asociada al envejecimiento y promueven una respuesta inmune más equilibrada, reduciendo la susceptibilidad a infecciones y enfermedades crónicas.
El cuidado del ecosistema intestinal emerge como un objetivo terapéutico preventivo prioritario para promover una longevidad saludable y funcional junto con un estilo de vida saludable que incluya una buena alimentación, actividad física y reducción del estrés.
Fuentes
Zhuang K, Luo H, Zeng M, Chan SCL, Gong M, Wang Y. Effects of probiotics, prebiotics, and synbiotics on gut microbiota in older adults: a systematic review and meta-analysis of randomized controlled trials. Nutr J. 2025 Sep 29;24(1):147. doi: 10.1186/s12937-025-01218-1. PMID: 41023690; PMCID: PMC12482033.
Envejecimiento y salud. Organización Mundial de la Salud. (2025). https://www.who.int/es/news-room/fact-sheets/detail/ageing-and-health?utm_source=chatgpt.com
Bradley E, Haran J. The human gut microbiome and aging. Gut Microbes. 2024 Jan-Dec;16(1):2359677. doi: 10.1080/19490976.2024.2359677. Epub 2024 Jun 3. PMID: 38831607; PMCID: PMC11152108.
Handajani YS, Turana Y, Hengky A, Hamid G, Schroeder-Butterfill E, Kristian K. Probiotics supplementation or probiotic-fortified products on sarcopenic indices in older adults: systematic review and meta-analysis from recent randomized controlled trials. Front Aging. 2024 Feb 2;5:1307762. doi: 10.3389/fragi.2024.1307762. PMID: 38370462; PMCID: PMC10873954.
Ku S, Haque MA, Jang MJ, Ahn J, Choe D, Jeon JI, Park MS. The role of Bifidobacterium in longevity and the future of probiotics. Food Sci Biotechnol. 2024 Jul 11;33(9):2097-2110. doi: 10.1007/s10068-024-01631-y. PMID: 39130652; PMCID: PMC11315853.
Alonso-Allende J, Milagro FI, Aranaz P. Health Effects and Mechanisms of Inulin Action in Human Metabolism. Nutrients. 2024 Sep 2;16(17):2935. doi: 10.3390/nu16172935. PMID: 39275251; PMCID: PMC11397174.
Fusco W, Lorenzo MB, Cintoni M, Porcari S, Rinninella E, Kaitsas F, Lener E, Mele MC, Gasbarrini A, Collado MC, et al. Short-Chain Fatty-Acid-Producing Bacteria: Key Components of the Human Gut Microbiota. Nutrients. 2023; 15(9):2211. https://doi.org/10.3390/nu15092211
Wu YL, Xu J, Rong XY, Wang F, Wang HJ, Zhao C. Gut microbiota alterations and health status in aging adults: From correlation to causation. Aging Med (Milton). 2021 Jun 24;4(3):206-213. doi: 10.1002/agm2.12167. PMID: 34553118; PMCID: PMC8444961.
Hou K, Wu ZX, Chen XY, Wang JQ, Zhang D, Xiao C, Zhu D, Koya JB, Wei L, Li J, Chen ZS. Microbiota in health and diseases. Signal Transduct Target Ther. 2022 Apr 23;7(1):135. doi: 10.1038/s41392-022-00974-4. PMID: 35461318; PMCID: PMC9034083.
Álvarez, J., Fernández Real, J. M., Guarner, F., Gueimonde, M., Rodríguez, J. M., Saenz de Pipaón, M., et al. (2021). Microbiota intestinal y salud. Gastroenterología y Hepatología, 44(7), 519-535. doi:10.1016/j.gastrohep.2021.06.002